
垃圾资源化的方法是
A.填埋 B.焚烧 C.堆肥 D.分类回收
科目:高中化学 来源:2014~2015学年江西四校9月联考高二化学试卷(解析版) 题型:填空题
(12分)氨是最重要的氮肥,是产量最大的化工品之一。德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4KJ/mol.他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4KJ/mol.他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)
2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时, N2和H2的转化率比是 。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量 ,密度 。(填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将 (填“正向”“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将 (填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度 (填“大于”“小于”或 “等于”)原来的2倍。
查看答案和解析>>
科目:高中化学 来源:2014秋贵州省遵义市高二上学期期中化学(文)试卷(解析版) 题型:选择题
碘酒是一种常用的外用消毒药,关于它的消毒原理说法正确的是
A.溶解细菌 B.氧化细菌,使蛋白质变性
C.使细菌缺氧而死 D.使细菌缺水而死
查看答案和解析>>
科目:高中化学 来源:2014秋贵州省遵义市高二上学期期中化学(文)试卷(解析版) 题型:选择题
葡萄糖作为营养剂供给人体能量,在体内发生主要的反应是
A.氧化反应 B.取代反应
C.加成反应 D.聚合反应
查看答案和解析>>
科目:高中化学 来源:2014秋贵州省遵义市高二上学期期中化学(文)试卷(解析版) 题型:选择题
硬铝是制造飞机和宇宙飞船的理想材料,下列哪一项不应该是硬铝的性能
A.加工性差 B.强度高 C.抗腐蚀 D.密度小
查看答案和解析>>
科目:高中化学 来源:2014秋福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
化学与生活息息相关,下列做法不正确的是
A.将废旧电池集中统一处理以防止重金属污染
B.对垃圾进行分类投放、分类回收、分类处理与再利用
C.用甲醛的水溶液浸泡海产品,防腐保鲜
D.按食品卫生标准严格控制食品添加剂(防腐剂等)的用量
查看答案和解析>>
科目:高中化学 来源:2014秋湖北省武汉市高二上学期期中联考化学试卷(解析版) 题型:填空题
(12分)中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
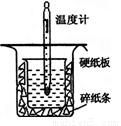
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_________,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”),简述理由: 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
2 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
3 | 25.1 | 25.1 | 25.1 | 27.1 | 2.0 |
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),根据计算结果,写出该中和反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:填空题
(10分)某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
实验编号 | 0.01mol·L-1 酸性KMnO4溶液 | 0.1mol·L-1 H2C2O4溶液 | 水 | 1mol·L-1 MnSO4溶液 | 反应温度 /℃ | 反应时间 |
I | 2mL | 2mL | 0 | 0 | 20 | 125 |
II | ____mL | ____mL | 1mL | 0 | 20 | 320 |
III | ____mL | __ _mL | ___mL | 0 | 50 | 30 |
IV | 2mL | 2mL | 0 | 2滴 | 20 | 10 |
已知:反应的方程式(未配平):KMnO4 + H2C2O4 + H2SO4 —— K2SO4 + MnSO4 + CO2↑+ H2O
(1)实验记时方法是从溶液混合开始记时,至___ ___ __时记时结束。
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响。请在上表空格中填入合理的实验数据。
(3)从实验数据分析,实验I和IV研究________对反应的影响。
(4)请配平上面的化学方程式:
KMnO4 + H2C2O4 + H2SO4= K2SO4 + MnSO4 + CO2↑+ H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com