
(15分)高铁酸钾(K2FeO4)是一种绿色氧化剂,在许多领域展现出广阔的应用前景。
(1)湿法制备K2FeO4:在KOH溶液中,用KC10直接氧化Fe(NO3)3即可制得K2FeO4。该反应的离子方程式为_________________________________。
(2)测定K2FeO4:样品纯度:i.称取样品mg,加入到盛有过量碱性亚铬酸钠[NaCr(OH)4]溶液的锥形瓶中充分反应;ii.将所得铬酸钠(Na2CrO4)溶液酸化;iii.在所得Na2Cr2O7溶液中加入8—9滴二苯胺磺酸钠溶液作指示剂,用c mol·L-1(NH4)2Fe(SO4)2溶液滴定至终点,消耗溶液体积为V mL。整个过程中发生的反应如下:
i. Cr(OH)4- + FeO42 -+  = Fe(OH)3 (H2O)3↓+ CrO42 -+
= Fe(OH)3 (H2O)3↓+ CrO42 -+
ii.2CrO42 -+2H+=Cr2O72 -+H2O;
iii.Cr2O72 -+6Fe2++14H+=2Cr3++6Fe3++7H2O
①配平方程式i;
②利用上述数据计算该样品的纯度为________________(用含字母的代数式表示)。
(3)高铁酸盐在水溶液中有四种含铁形体。25 ℃时,它们的物质的量分数随pH的变化如图所示:
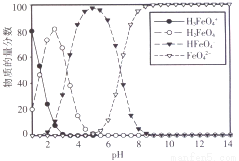
i.pH=2.2时,溶液中主要含铁形体浓度的大小关系为________;为获得尽可能纯净的高铁酸盐,pH应控制在______________。
ii.已知H3FeO4+ 的电离常数分别为:K1=2.51×10-2,K2=4.16×10-4,K3=5.01×10-8,当pH=4时,溶液中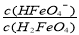 = 。
= 。
iii.向pH=6的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为______________。
(4)某新型电池以金属锂为负极,K2FeO4为正极,溶有LiPF6的有机溶剂为电解质。工作时Li+通过电解质迁移人K2FeO4晶体中,生成K2Li2FeO4。该电池的正极反应式为______________.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年湖北省等高三下学期期中四校联考化学试卷(解析版) 题型:选择题
在1升密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:(1)2A(g) 2B(g)+C(g);(2)A(g)
2B(g)+C(g);(2)A(g) C(g)+D(g)。当达到平衡时,测得c(A)=2.5 mol·L-1,c(C)=2.0 mol·L-1。则下列说法中正确的是:
C(g)+D(g)。当达到平衡时,测得c(A)=2.5 mol·L-1,c(C)=2.0 mol·L-1。则下列说法中正确的是:
A.达到平衡时A的总转化率为40%
B.达到平衡时c(B)为1.0 mol·L-1
C.达到平衡时c(B)=2c(D)
D.达到平衡时c(D)为0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省哈尔滨市高三二模考试理综化学试卷(解析版) 题型:填空题
[化学——选修3]物质结构与性质:(15分)有A、B、C、D、E五种元素。其相关信息如下:

请回答下列问题。
(1)写出E元素原子基态时M层的电子排布式 。
(2)C元素单质分子中含有δ和∏键的键数之比为 。
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是: :C2A4分子中c原子轨 道的杂化类型是 。
(4)A、C、E三种元素可形成:【E(CA3)4】2+配离子,其中存在的化学键类型有 (填序号):
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若【E(CA3)4】2+具有对称的空间构型.且当【E(CA3)4】2+中的两个CA3分子被两个Cl一取代时.能得到两 种不同结构的产物,则【E(CA3)4】2+的空间构型为 (填序号)。
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)B与D可形成离子化合物.其晶胞结构如图所示。其中D离子的配位数为 .若该晶体的密 度为a g·cm-3,则该晶胞中距离最近的B和D之间的距离是 cm(写出表达式即可,NA代表阿伏加得罗常数)
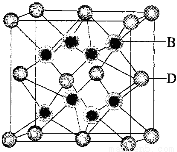
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:实验题
(15分)碱式碳酸钴 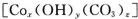 常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
常用作电子材料、磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验。
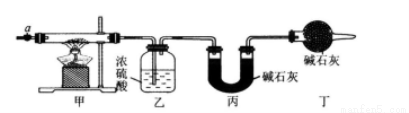
(1)请完成下列实验步骤:
①称取3.65 g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中_______(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通人空气数分钟的目的是___________________________________.
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的_______(填字母)连接在_______(填装置连接位置)。
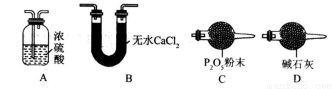
(4)若按正确装置进行实验,测得如下数据。
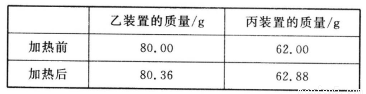
则该碱式碳酸钴的化学式为______________。
(5)含有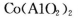 的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为_______。
的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为_______。
(6) 常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取
常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取 的一种工艺如下:
的一种工艺如下:

①净化除杂时,加入H2O2发生反应的离子方程式为____________________________.
②加入CoCO3 调pH为5.2~7.6,则操作1获得的滤渣成分为_____________________.
③加盐酸调整pH为2~3的目的为__________________________________________.
④操作Ⅱ过程为蒸发浓缩、______________(填操作名称)、过滤。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期三调考试化学试卷(解析版) 题型:选择题
有关化学资源的合成、利用与开发的叙述合理的是
A.大量使用化肥和农药,能不断提高农作物产量
B.通过有机合成,可以制造出比钢铁更强韧的新型材料
C.安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率
D.开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三下学期期中考试理综化学试卷(解析版) 题型:选择题
根据原子结构及元素周期律的知识,下列推断正确的是
A.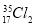 与
与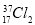 氧化能力相近,二者互为同位素
氧化能力相近,二者互为同位素
B.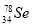 与
与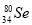 所含质子数相同,中子数不同
所含质子数相同,中子数不同
C.同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱
D.同周期主族元素形成的简单离子半径随核电荷数的增大而减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三4月阶段测试理综试卷化学试卷(解析版) 题型:选择题
某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验:
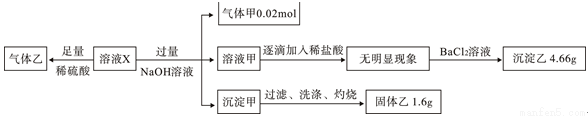
则下列说法正确的是
A.若含有Fe3+,则一定含有Cl-
B.SO42-、NH4+一定存在,NO3-、Cl–可能不存在
C.CO32-、Al3+、K+一定不存在
D.气体甲、沉淀甲一定为纯净物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省金华十校高三下学期高考模拟(4月)理综化学试卷(解析版) 题型:选择题
化学与科学、社会、技术和环境密切相关。下列有关说法中错误的是
A.目前科学家已制得单原子层锗,其电子迁移率是硅的10倍,有望用于制造高能计算机芯片
B.2014年在西非国家爆发了埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
C.2014年德美科学家因开发超分辨荧光显微镜获诺贝尔化学奖,使光学显微镜分辨率步入了纳米时代。利用此类光学显微镜可以观察活细胞内蛋白质等大分子
D.绿色化学期望利用化学原理从源头消除污染,在生产过程中充分利用原料,实现零排放
查看答案和解析>>
科目:高中化学 来源: 题型:
关于活化分子说法错误的是()
A. 发生有效碰撞的分子一定是活化分子
B. 活化分子间的碰撞一定是有效碰撞
C. 能发生有效碰撞的分子必须具有相当高的能量
D. 使用催化剂能改变分子的活化能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com