
| A. | 浓度均为0.1 mol•L-1的氨水和盐酸等体积混合后:c(H+)=c(OH-)+c(NH3•H2O) | |
| B. | 等浓度的碳酸钠、碳酸氢钠溶液混合后:c(CO${\;}_{3}^{2-}$)<c(HCO${\;}_{3}^{-}$) | |
| C. | 在NaHB溶液中一定有:c(Na+)=c(HB-)+2c(B2-) | |
| D. | Na2CO3溶液中:2c(Na+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(H2CO3) |
分析 A.二者恰好反应生成氯化铵,根据氯化铵溶液中的质子守恒判断;
B.缺少溶液浓度,无法判断混合液中碳酸根离子、碳酸氢根离子的浓度大小;
C.根据NaHB溶液中的物料守恒判断;
D.根据碳酸钠溶液中的物料守恒判断.
解答 解:A.浓度均为0.1 mol•L-1的氨水和盐酸等体积混合后生成氯化铵,根据质子守恒可得:c(H+)=c(OH-)+c(NH3•H2O),故A正确;
B.未知两溶液的体积关系,不能确定离子浓度大小,故B错误;
C.NaHB溶液中物料守恒式为:c(Na+)=c(HB-)+c(H2B)+c(B2-),故C错误;
D.溶液中,根据物料守恒可得:c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)],故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理、电荷守恒、物料守恒及质子守恒的含义为解答关键,试题充分考查了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 4HCl+MnO2$\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O | |
| B. | 2HCl+CaCO3=CaCl2+CO2+H2O | |
| C. | 2HCl+Zn=ZnCl2+H2↑ | |
| D. | HCl+AgNO3=AgCl↓+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 应量取盐酸体积/mL | 应选用容量瓶的规格/mL |
| 2.1mL | 250mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状态时,22.4L的CO2 | B. | 200g49%的H3PO4 | ||
| C. | 32g 的SO2气体 | D. | 3.01×1023个O2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
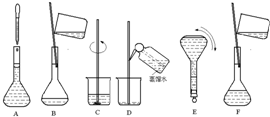 如图表示配制 100mL 0.100ol•L-1 Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:
如图表示配制 100mL 0.100ol•L-1 Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以下离子可存在于能使酚酞变红的溶液中:Na+,Ba2+,NO3-,Cl- | |
| B. | 以下离子可存在于含有0.1mol•L-1 Fe3+的溶液中:K+,Mg2+,I-,SO42- | |
| C. | 用氯水作为水的消毒剂的原理为:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 纯碱用于清洁厨具是由于它溶于水呈碱性的缘故:HCO3-+H2O?OH-+H2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com