
硝基苯甲酸乙酯在OH-存在下发生水解反应:
O2NC6H4COOC2H5+OH-O2NC6H4COO-+C2H5OH
两种反应物的初始浓度均为0.050 mol·L-1,15 ℃时测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。回答下列问题:
| t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
| α/% | 0 | 33.0 | 41.8 | 48.8 | 58.0 | 69.0 | 70.4 | 71.0 | 71.0 |
(1)列式计算该反应在120~180 s与180~240 s 区间的平均反应速率________、________;比较两者大小可得出的结论是____________________。
(2)列式计算15 ℃时该反应的平衡常数________。
(3)为提高O2NC6H4COOC2H5的平衡转化率,除可适当控制反应温度外,还可采取的措施有________(要求写出两条)。
(1)v= =
=
7.3×10-5 mol·L-1·s-1
v= =
=
5.8×10-5mol·L-1·s-1
随着反应的进行,反应物浓度降低,反应速率减慢
(2)K= =6.0或K=
=6.0或K=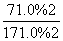 =6.0
=6.0
(3)增加OH-的浓度、移去产物
[解析] (1)反应过程中硝基苯甲酸乙酯浓度的变化量等于其起始浓度与转化率的乘积,再利用求反应速率的计算公式可求出两个时间段内的平均反应速率分别为7.3×10-5 mol·L-1·s-1、5.8×10-5 mol·L-1·s-1,由此可得出的结论是随着反应的进行,反应物浓度减小导致反应速率降低。(2)反应时间达到700 s时,硝基苯甲酸乙酯的转化率不再随时间的变化而发生变化,即反应在700 s时达到平衡。此时体系内两种产物浓度为0.05 mol/L×71%,反应物浓度为0.05 mol/L×29%,由此可求出该反应的平衡常数。(3)根据可逆反应的特点可知增加OH-的浓度、及时地移去产物均可以增大硝基苯甲酸乙酯的转化率。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
为了确定某物质是否变质,所选试剂(括号内物质)错误的是
A.Na2SO3是否被氧化(BaCl2) B.FeCl2是否被氧化(KSCN)
C.KI是否被氧化(淀粉溶液) D.氯水是否失效(pH试纸)
查看答案和解析>>
科目:高中化学 来源: 题型:
在Al2O3+N2+3C=2AlN+3CO 反应中,氧化剂与转移电子方向和数目是
A.Al2O3 N→Al 3 B.Al2O3 C→Al 12 C.N2 C→N 6 D.N2 N→C 5
查看答案和解析>>
科目:高中化学 来源: 题型:
将3.9gNa2SO4和Na2CO3的混合物溶于水得到溶液A,在A中加入足量的一定浓度的BaCl2溶液20.0mL,然后过滤得沉淀B和滤液C.在C中加足量AgNO3溶液,又生成11.48g沉淀,向B中加入足量稀硫酸,沉淀增加0.36g.计算:
(1)氯化钡溶液的物质的量浓度;
(2)原混合物中硫酸钠的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)  N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
| A | B |
|
|
|
| 升高温度,平衡常数减小 | 0~3 s内,反应速率为 v(NO2)=0.2 mol·L-1 |
| C | D |
|
|
|
| t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:
(1)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 kJ。该反应的热化学方程式为____________________________________________。
(2)反应AX3(g)+X2(g)AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

①列式计算实验a从反应开始至达到平衡时的反应速率v(AX5)=______________________。
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为____________(填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:b________________________________________________,c____________________________________________。
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为______________;实验a和c的平衡转化率:αa为________,αc为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中通入X并发生反应:2X(g)Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示,下列叙述正确的是( )
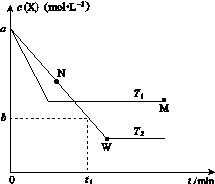
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= mol·L-1·min-1
mol·L-1·min-1
C.M点的正反应速率v正大于N点的逆反应速率v逆
D.M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)  M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
| 实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
| n(X) | n(Y) | n(M) | |||
| ① | 700 | 0.40 | 0.10 | 0.090 | |
| ② | 800 | 0.10 | 0.40 | 0.080 | |
| ③ | 800 | 0.20 | 0.30 | a | |
| ④ | 900 | 0.10 | 0.15 | b | |
下列说法正确的是( )
A.实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com