
二氧化锰可用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。
Ⅰ(1)锌—锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。电池的总反应式为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)。
电池的正极反应式为________________________________
Ⅱ某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰。
①将干电池剖切、分选得到黑色混合物(主要成分为MnO2)洗涤、过滤、烘干。
②将上述固体按固液体积比2:9加入浓盐酸、加热,反应完全后过滤、浓缩。
③向上述溶液中加入Na2CO3溶液,边加边搅拌,再过滤即可得到碳酸锰。
(2)在第②步中,将上述固体与浓盐酸混合的目的是________________________________
(3)有人认为,将第③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成。请写出加入NH4HCO3溶液时发生的离子反应方程式:
_______________________________________
Ⅲ 湿法炼锰即电解硫酸锰溶液法。电解锰的生产过程分为化合浸取、氧化净化及沉淀除杂、产品回收。其生产工艺流程如下:
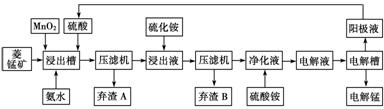
已知:①菱锰矿中主要成份是碳酸锰,主要杂质是Fe2+、Co2+、Ni2+。
②生成氢氧化物的pH如下表:(若某离子浓度小于等于10-5mol/L,则认为完全沉淀)
| 物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 |
| 完全沉淀pH | 9.7 | 8.4 | 8.2 | 9.8 |
③有关难溶氢氧化物和硫化物pKsp数据(pKsp=-lgKsp):
| 难溶物质 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | NiS | CoS |
| pKsp | 38.55 | 15.26 | 14.7 | 18.49 | 20.40 |
(4)菱锰矿粉与硫酸反应的化学方程式是________________________________。
(5)使用氨水的目的是调节pH值在________之间(填pH范围,精确到小数点后1位数字)。
在“浸出液”中加入(NH4)2S(硫化铵)的目的是_________________________________
(6)电解槽中使用的是惰性电极板,电解反应方程式为_________________________
【知识点】难溶电解质的溶解平衡及沉淀转化的本质、制备实验方案的设计
【答案解析】 (每空2分)(1)2MnO2+2e-+H2O=2OH-+Mn2O3 (2)将MnO2还原成Mn2+
(3)Mn2++2HCO3-=MnCO3↓+CO2↑+H2O (4)MnCO3+H2SO4=MnSO4+H2O+CO2↑
(5)3.8~8.3 作沉淀剂,生成NiS沉淀 (6)2MnSO4+2H2O  2H2SO4+O2↑+2Mn
2H2SO4+O2↑+2Mn
解析:(1)锌—锰碱性电池的总反应式为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s),
Zn化合价升高,失电子,作负极;MnO2中的Mn化合价降低,得电子,作正极,根据总反应拆成两个半反应,电池的正极反应式为:2MnO2+2e-+H2O=2OH-+Mn2O3
(2)浓盐酸与二氧化锰发生氧化还原反应,生成氯气和氯化锰,以便于加入碳酸钠后可以生成碳酸锰沉淀;
(3)加入NH4HCO3溶液时,生成气体,离子方程式为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O
(4)菱锰矿粉主要成分是碳酸锰,与硫酸反应生成硫酸锰、水和二氧化碳,化学方程式是:
MnCO3+H2SO4=MnSO4+H2O+CO2↑
(5)二氧化锰MnO2具有氧化性,能将菱锰矿的硫酸浸取液中的Fe2+氧化为Fe3+; 氨水可以将铁离子沉淀,氢氧化铁的Ksp=c3(OH-)•c(Fe3+),铁离子完全沉淀时,铁离子的浓度是1×10-5mol/L,此时c(OH-)=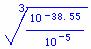 = 10-11.2mol/L,所以pH=3.8,所以将铁离子沉淀完全,但是锰离子未沉淀的范围是3.8~8.3,此范围内Co2+已经沉淀完全,所以再加入硫化铵将Ni2+沉淀;
= 10-11.2mol/L,所以pH=3.8,所以将铁离子沉淀完全,但是锰离子未沉淀的范围是3.8~8.3,此范围内Co2+已经沉淀完全,所以再加入硫化铵将Ni2+沉淀;
(6)根据电解池的工作原理,电解硫酸锰酸性溶液生成二氧化锰、硫酸和氢气,电解反应方程式为:
2MnSO4+2H2O  2H2SO4+O2↑+2Mn
2H2SO4+O2↑+2Mn
【思路点拨】本题是一道实验方案设计的工艺流程题目,考查学生各方面的综合知识能力,尤其是第(5)题,二氧化锰将亚铁氧化,再调节PH的计算难度大;


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实,其反应的化学方程式为:2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g) 。 下列叙述正确的是( )
CH3CH2OH(g)+3H2O(g) 。 下列叙述正确的是( )
A.当v(CO2)=2v(CH3CH2OH)时,反应一定达到平衡状态
B.当平衡向正方向移动时,平衡常数一定增大
C.增大压强,可提高CO2和H2的转化率
D.相同条件下,2 mol氢原子所具有的能量等于1 mol氢分子所具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
a1,a2分别为A在两个恒容容器中平衡体系A(g) 2B(g) 和A(g)
2B(g) 和A(g) B(g)的转化率,在温度不变的情况下,均增加A(g)的物质的量,则 a1_______,a2______,(填“减小”或“增大”或“不变”)
B(g)的转化率,在温度不变的情况下,均增加A(g)的物质的量,则 a1_______,a2______,(填“减小”或“增大”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式( )
A.浓盐酸与铁屑反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
B.钠与CuSO4溶液反应:2Na + Cu2+ = Cu↓+ 2Na+
C.NaHCO3溶液与稀H2SO4反应:CO32-+ 2H+ = H2O + CO2↑
D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
运用有关概念判断下列叙述正确的是( )
A.1molH2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
C.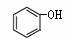 和
和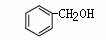 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中所含的少量杂质的方法正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 提纯方法 |
| A | BaSO4 | BaCO3 | 水 | 溶解、过滤、洗涤 |
| B | CO2 | SO2 | 饱和Na2CO3溶液 | 洗气 |
| C | 乙酸乙酯 | 乙酸 | 稀NaOH溶液 | 混合振荡、静置分液 |
| D | 蛋白质 | 葡萄糖 | 浓(NH4)2SO4溶液 | 盐析、过滤、洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下在容积恒定的密闭容器中,进行反应A(s)+2B(g)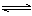 C(g)+D(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( )
C(g)+D(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( )
①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④B的物质的量浓度
A.①④ B.只有②③ C.②③④ D.只有④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com