
| A. | 2:4:3 | B. | 2:4:5 | C. | 2:4:7 | D. | 3:5:8 |
分析 涉及的反应有2Na2O2+2CO2=2Na2CO3+O2,2H2+O2=2H2O,4NO+3O2+2H2O=4HNO3,得到浓度为70%的硝酸溶液,设硝酸为70g,则水为30g,则:n(HNO3)=$\frac{70g}{63g/mol}$=$\frac{10}{9}$mol,n(H2O)=$\frac{30g}{18g/mol}$=$\frac{5}{3}$mol,根据方程式结合质量守恒计算.
解答 解:设得到70%的硝酸100g,70%的硝酸中n(HNO3)=$\frac{70g}{63g/mol}$=$\frac{10}{9}$mol,n(H2O)=$\frac{30g}{18g/mol}$=$\frac{5}{3}$mol,其中n(H):n(N):n(O)=(2×$\frac{5}{3}$mol+$\frac{10}{9}$mol):$\frac{10}{9}$mol:($\frac{5}{3}$mol+3×$\frac{10}{9}$mol)=4:1:4.5,
通过足量Na2O2后,n(O2)=$\frac{1}{2}$n(CO2),n(H2):n(NO):n(O2)=$\frac{4}{2}$:1:$\frac{4.5-1}{2}$=2:1:1.75,则n(H2):n(NO):n(CO2)=2:1:3.5,
即:n(NO):n(H2):n(CO2)=2:4:7,
答案选C.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| B. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | |
| C. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+4H++2MnO4-═5SO42-+2Mn2++2H2O | |
| D. | 向AlCl3溶液滴入过量氨水:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
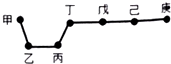
| A. | 单质甲与单质乙充分反应一定都可以生成多种化合物 | |
| B. | 简单气态氢化物的稳定性:庚>己>戊>丁 | |
| C. | 可以通过分别电解熔融的金属氯化物的方法冶炼乙和丙的单质 | |
| D. | 因为庚元素的非金属性最强,所以庚的最高价氧化物对应水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

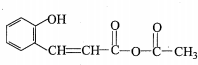 ,G
,G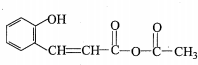

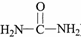 )氮原子上的氢原子可以像A上的氢原子那样与C发生加成反应,再缩聚成高分子化合物.写出尿素与C在一定条件下生成线性高分子化合物的化学方程式
)氮原子上的氢原子可以像A上的氢原子那样与C发生加成反应,再缩聚成高分子化合物.写出尿素与C在一定条件下生成线性高分子化合物的化学方程式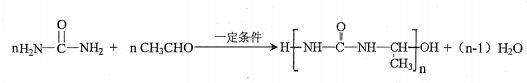
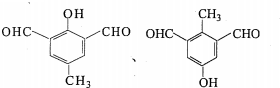 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A | 切开金属钠,钠表面的银白色会逐渐变暗 | Na在空气中会生成Na2O2 |
| B | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| C | SO2通入酸性KMnO4溶液,溶液褪色 | SO2具有漂白性 |
| D | 将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的$\frac{2}{3}$处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 | 从原料的充分利用和减少污染物的排放等方面考虑,该实验对工业生产硝酸有重要启示 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备其单质 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
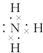 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
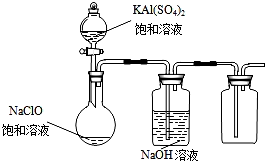 NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业.
NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
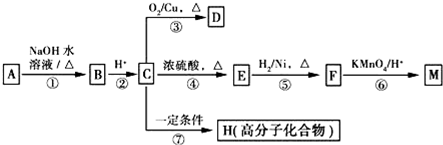
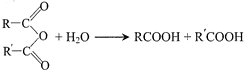
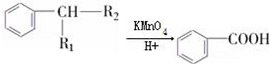 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)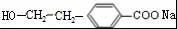 .
.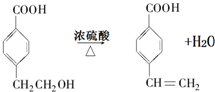 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com