
已知:Ksp(AgCl ) = 1.8 × 10-10 ,Ksp(AgI) = 1.5 × 10-16 ,Ksp(Ag2CrO4) =2.0 × 10-12,则在相同温度下,下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
) = 1.8 × 10-10 ,Ksp(AgI) = 1.5 × 10-16 ,Ksp(Ag2CrO4) =2.0 × 10-12,则在相同温度下,下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl>AgI>Ag2CrO4 B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI D.Ag2CrO4>AgI>AgCl
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届贵州省高三上半期考试化学试卷(解析版) 题型:选择题
将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中金属阳离子情况不可能是( )
A.只含 Cu2+、Fe2+、Zn2+ B.只含 Zn2+
C.只含 Fe2+、Zn2+ D.只含 Cu2+、Fe3+、Zn2+
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次质检化学试卷(解析版) 题型:实验题
高氯酸铵可用于火箭推进剂,实验室可由NaClO等原料制取(部分物质溶解度如下图),其实验流程如下:
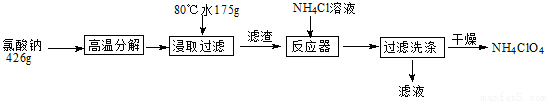
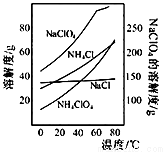
(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为_____________________。
(2)80℃时浸取液冷却至0℃过滤,滤渣的主要成分为_________________(写化学式)。
(3)反应器中加入氯化铵饱和溶液发生反应的离子方程式为_____________________
(4)已知:2NH4C1O4 N2+2O2↑+C12↑+4H2O,现可提供下列试剂:
N2+2O2↑+C12↑+4H2O,现可提供下列试剂:
a.饱和食盐水 b.浓H2SO4 c.NaOH溶液 d.CuO e.Cu
利用下图装置对高氯酸 铵热分解产生的三种气体进行分别吸收或收集。
铵热分解产生的三种气体进行分别吸收或收集。

①E中收集到的气体可能是__________(填化学式)。
②A、B、C中盛放的药品依次可以是_________(选填:I、II、III)。
I.a、b、d II.c、b、d III.c、b、e
(5)过滤用到的主要玻璃仪器是_______________。
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上第二次月考化学试卷(解析版) 题型:选择题
室温下,用0.1 mol/L HCl溶液滴定10 mL 0.1 mol/L Na2CO3溶液,滴定曲线如图所示。下列说法正确的是
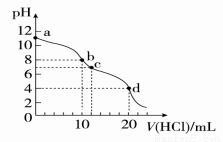
A.a点时:c(Na+)>c(CO32-)>c (HCO3-)>c(OH-)
B.b点时:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3)
C.水电离程度由大到小的顺序为:a>b>c>d
D.d点时:c(H+)>c(HCO3-)=c(CO32-)
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上第二次月考化学试卷(解析版) 题型:选择题
能正确 表示下列反应的离子方程式是
表示下列反应的离子方程式是
A.CuCl2溶液中加入少量氨水:Cu2++2OH-=Cu(OH)2↓
B.向酸性KMnO4溶液中通入SO2:3SO2+2MnO4-+4OH-=2MnO 2↓+3SO42-+2H2O
2↓+3SO42-+2H2O
C.向碳酸氢钙溶液中加足量澄清石灰水:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.铝溶于氢氧化钠溶液:Al+2OH-+H2O=AlO2-+2H2↑
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上第四次质检化学试卷(解析版) 题型:实验题
半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O (g)。半水煤气经过下列步骤转化为 合成氨的原料。完成下列填空:
合成氨的原料。完成下列填空:
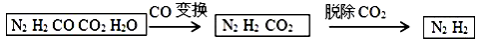
(1)半水煤气含有少量硫化氢。将半水煤气样品通入 溶液中(填写试剂名称),出现 ,可以证明有硫化氢存在。
(2)写出半水煤气在铜催化下实现CO变换的反应方程式 ;若半水煤气中V(H2): V(CO): V(N2)=9:7:4,经CO变换后的气体中: V(H2): V(N2)=__________。
V(H2): V(N2)=__________。
(3)碱液吸收法是脱除二氧化碳的方法之一。有一吸收了二氧化碳的氢氧化钠洛液,为测定其溶液组成,采用双指示剂法进行滴定。
步骤:用移液管量取V0mL的该溶液于锥形瓶中,先滴入1-2滴酚酞做指示剂,滴定达到终点时用去c mol.L-1的标准盐酸溶液VlmL,此时再向溶液中滴入1-2滴__________做指示剂,达到滴定终点时又用去V2mL标准盐酸溶液。
第二次滴定达到终点时的现象是______________________。
数据处理:通过Vl和V2的相对大小可以定性也可定量判断溶液的组成。
若V1>V2,写出此时的溶质的化学式_______________。
若2V1=V2,写出此时溶液中离子浓度由大到小的顺序_________________。
讨论:若V1<V2,在第一次滴定时未用标准盐酸润洗酸式滴定管,第二次滴定前发现并纠正了错误,则____________(填化学式)浓度偏大。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上第四次质检化学试卷(解析版) 题型:选择题
其他条件不变,升高温度下列数据不一定增大的是( )
A.可逆反应的化学平衡常数K B.0.1 mol/L CH3COONa溶液的pH
C.水的离子积常数KW D.弱电解质的电离程度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:填空题
室温下将a mL三种一元酸分别和NaOH溶液等体积混合,实验数据如下:
组别 | c(一元酸) | c(NaOH) / mol·L-1 | 混合溶液的pH |
甲 | c(HX)=0.1 mol·L-1 | 0.1 | pH = 10 |
乙 | c(HY)=0.1 mol·L-1 | 0.1 | pH = 7 |
丙 | c(HZ)=0.1 mol·L-1 | 0.1 | pH = 9 |
(1)根据表中数据比较HX、HY、HZ三种酸的酸性由强到弱的顺序为_________,丙组实验发生反应的离子方程式为 ,所得溶液中由水电离出的c(OH-)= mol·L-1。
(2)部分实验反应过程中的pH变化曲线如下图:
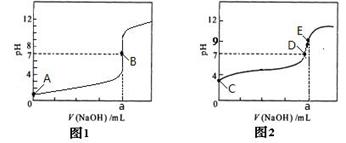
①表示乙组实验的pH变化曲线是________________(填“图1”或“图2”)
②以上两图中表示溶液恰好完全反应的点是________________。
(3)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,所得溶液均呈中性。
①浓度为1.0×10-3 mol·L-1的氨水b L
②c(OH-)=1.0×10-3 mol·L-1的氨水c L
③c(OH-)=1.0×10-3 mol·L-1的氢氧化钡溶液d L。则a、b、c、d的大小关系是_________________。
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是__________(填“A”或“B”);设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2.则m1__________m2(填“<”、“=”、“>”)
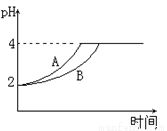
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com