
| A. | 苯的分子式为C6H6 | B. | 乙酸乙酯易溶于水 | ||
| C. | 乙醇可用作燃料 | D. | 加热可以使蛋白质变性 |
科目:高中化学 来源: 题型:多选题
| A. | 向0.1molFeI2溶液中滴加少量氯水,反应中有0.3mol电子转移 | |
| B. | 向溴水中加入足量氯化亚铁能使溶液变成无色 | |
| C. | 向NaClO溶液中通入少量CO2的离子方程式:ClO-+CO2+H2O═HClO+HCO3- | |
| D. | 能使pH试纸显深红色的溶液,Fe3+、Cl-、Ba2+、Br-能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
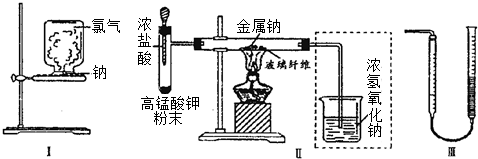
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠可用于治疗胃酸过多,作胃酸中和剂 | |
| B. | 氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 | |
| C. | 碳酸钠固体中混有少量碳酸氢钠,可用加热的方法除去 | |
| D. | 质量相等的碳酸钠和碳酸氢钠分别与足量盐酸反应,后者产生气体少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加热的方法分离沙子和氯化铵晶体 | |
| B. | 用洁净的铂丝蘸取氯化钠溶液在无色火焰上灼烧,焰色呈黄色 | |
| C. | 胆矾受热变成白色粉末 | |
| D. | 熔融的氯化钠导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

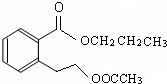 或
或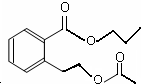 .
.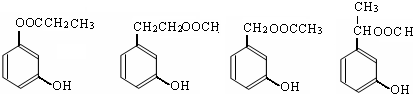 (其中一种).
(其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
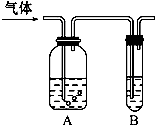 如图把气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( )
如图把气体缓慢通过盛有足量试剂的试剂瓶A,在试管B中可以观察到明显现象的是( )| 选项 | 气怵 | A中试剤 | B中试剤 |
| A | SO2、CO2 | 酸性KMnO4溶液 | 品红溶液 |
| B | Cl2、HC1 | 浓硫酸 | KI淀粉溶液 |
| C | NH3、CO2 | 浓硫酸 | 酚酞试液 |
| D | CO2、HC1 | NaOH溶液 | 澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
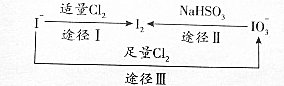 碘在地壳中主要以NaIO3的形式存在.在海水中主要以I-的形式存在.几种粒子之间有如图转化关系,根据如图转化关系推测下列说法不正确的是( )
碘在地壳中主要以NaIO3的形式存在.在海水中主要以I-的形式存在.几种粒子之间有如图转化关系,根据如图转化关系推测下列说法不正确的是( )| A. | 可用KI-淀粉试纸和食醋检验加碘盐中是否含有碘 | |
| B. | 在碘水中通入Cl2,发生反应的化学方程为5Cl2+I2+6H2O=2HIO3+10HCI | |
| C. | 由图可知氧化性的强弱顺序为Cl2>I2>IO3 | |
| D. | 途径Ⅲ中,若消耗1moICl2,反应中转移的电子为2moI |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
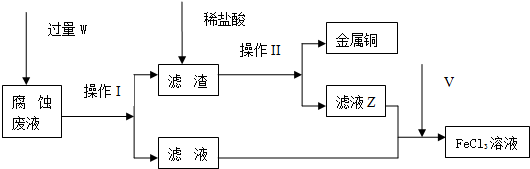
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com