
| A. | NH4Cl | B. | HCl | C. | MgCl2 | D. | CH4 |
科目:高中化学 来源: 题型:解答题
 ,名称是3,4-二甲基辛烷.
,名称是3,4-二甲基辛烷.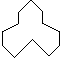 名称是环十二烷,1mol该烃完全燃烧,需消耗氧气18mol.
名称是环十二烷,1mol该烃完全燃烧,需消耗氧气18mol. 名称是3-甲基-4-乙基-3-己烯
名称是3-甲基-4-乙基-3-己烯 名称是2,2,3-三甲基戊烷
名称是2,2,3-三甲基戊烷查看答案和解析>>
科目:高中化学 来源: 题型:选择题
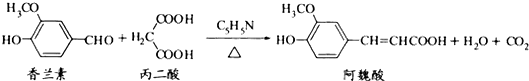
| A. | 与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物有2种 | |
| B. | 香兰素、阿魏酸均可与NaHCO3、NaOH溶液反应 | |
| C. | 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 | |
| D. | 香兰素、阿魏酸均可与溴水反应,且反应类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m+2-a | B. | n+m+a | C. | 2n+3m-a | D. | m+2n+2-a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
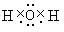 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3molH2+2molN2 | B. | 2molNH3+1molN2 | ||
| C. | 3molN2+1molH2 | D. | 0.1molNH3+0.95molN2+2.85molH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com