
 ZnSO4+SO2��+2H2O����ѡ�õ�ҩƷΪ18 mol/L������Һ��п����Ʒ����Һ����ˮ�����Ը��������Һ��Ũ���ᡢ����ͭ����ˮ����ͭ����ʯ�ҡ���ʾ���ٶ���������л�ԭ�ԣ�����������ͭ��Ӧ����E��Fװ�ö�ʹ�ã���ͬһװ�ÿɶ��ʹ�á�
ZnSO4+SO2��+2H2O����ѡ�õ�ҩƷΪ18 mol/L������Һ��п����Ʒ����Һ����ˮ�����Ը��������Һ��Ũ���ᡢ����ͭ����ˮ����ͭ����ʯ�ҡ���ʾ���ٶ���������л�ԭ�ԣ�����������ͭ��Ӧ����E��Fװ�ö�ʹ�ã���ͬһװ�ÿɶ��ʹ�á� 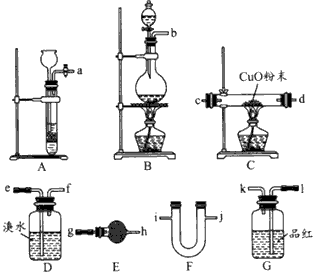
 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�찲ʡ�����и߶���ѧ�����п��Ի�ѧ�Ծ��Ծ��������棩 ���ͣ������
���仯�����й㷺��Ӧ�ã���SO2���ʵ��о��Ǹ��л�ѧ��ѧ��һ����Ҫ���ݡ�
I���Ա��о���һ����Ҫ���о�������������ĵ��ʼ����ֻ����ﰴ���±���ʾ�ֳ�3 �飬���2��������M�Ļ�ѧʽ�� ��
|
��1�� |
��2�� |
��3�� |
|
S (����) |
SO2��H2SO3��M��NaHSO3 |
SO3��H2SO4��Na2SO4�� NaHSO4 |
��ijУ��ѧѧϰС������ͼ��ʾ��ʵ��װ���о�SO2���廹ԭFe3+��Br2�ķ�Ӧ��

��1������ʵ�鷽������������ʵ������ȡ����SO2���� ��
A��Na2SO3��Һ��HNO3 B��Na2SO3����Ũ����
C���������ڴ�����ȼ�� D��ͭ���ȵ�Ũ����
��2��װ��C�������dz�ȥ�����SO2����ֹ��Ⱦ��������֪��������������Һ����SO2�� �����У������õ�Na2SO3��NaHSO3�Ļ����Һ�������£���ҺpH��n(SO32��)��n(HSO3��)�仯��ϵ���±�
|
n(SO32��)��n(HSO3��) |
91��9 |
1��1 |
9��91 |
|
pH |
8.2 |
7.2 |
6.2 |
������Һ��n(SO32��)��n(HSO3��) =10��1ʱ����Һ������Ũ�ȹ�ϵ��ȷ���� ��
A��c(Na+)+ c(H+)= 2c(SO32��)+ c(HSO3��)+ c(OH��)
B��c(Na+)��c(HSO3��)��c(SO32��)��c(OH��)��c(H+)
C��c(Na+)��c(SO32��)��c(HSO3��)��c(OH��)��c(H+)
��3��������װ����ͨ�������SO2��Ϊ����֤A��SO2��Fe3+������������ԭ��Ӧ������ȡA�з�Ӧ�����Һ�ֳ����ݣ������������̽��ʵ�飬�������۲��������ǵ�̽�����̣���ѡ�Լ���KMnO4��Һ��KSCN��Һ��BaCl2��Һ��ϡ���ᡢϡ���ᡢϡ�� �ᡢBa(NO3)2��Һ�����Ƶ���ˮ��
|
��� |
ʵ�鷽�� |
ʵ������ |
���� |
|
������ |
����һ����Һ�м���KMnO4��Һ��Һ |
�Ϻ�ɫ��ȥ |
SO2��Fe3+��Ӧ������Fe2+ |
|
������ |
���ڶ�����Һ�м��� |
|
SO2��Fe3+��Ӧ������Fe2+ |
|
������ |
���ڶ�����Һ�м��� |
|
SO2��Fe3+��Ӧ������SO42�� |
���������ٵó��Ľ����Ƿ���� ��ԭ�� ��
���������Ƶķ������뷽���۾��������ҵõ���Ӧ���ۣ����㽫�������������
��4��װ��B���ܱ���Br���Ļ�ԭ������SO2�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�갲��ʡ�����и���4���������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
���仯�����й㷺��Ӧ�ã���SO2���ʵ��о��Ǹ��л�ѧ��ѧ��һ����Ҫ���ݡ�
I���Ա��о���һ����Ҫ���о�������������ĵ��ʼ����ֻ����ﰴ���±���ʾ�ֳ�3 �飬���2��������M�Ļ�ѧʽ�� ��
|
��1�� |
��2�� |
��3�� |
|
S (����) |
SO2��H2SO3��M��NaHSO3 |
SO3��H2SO4��Na2SO4�� NaHSO4 |
��ijУ��ѧѧϰС������ͼ��ʾ��ʵ��װ���о�SO2���廹ԭFe3+��Br2�ķ�Ӧ��

��1������ʵ�鷽������������ʵ������ȡ����SO2���� ��
A��Na2SO3��Һ��HNO3 B��Na2SO3����Ũ����
C���������ڴ�����ȼ�� D��ͭ���ȵ�Ũ����
��2��װ��C�������dz�ȥ�����SO2����ֹ��Ⱦ��������֪��������������Һ����SO2�� �����У������õ�Na2SO3��NaHSO3�Ļ����Һ�������£���ҺpH��n(SO32��)��n(HSO3��)�仯��ϵ���±�
|
n(SO32��)��n(HSO3��) |
91��9 |
1��1 |
9��91 |
|
pH |
8.2 |
7.2 |
6.2 |
������Һ��n(SO32��)��n(HSO3��) =10��1ʱ����Һ������Ũ�ȹ�ϵ��ȷ���� ��
A��c(Na+)+ c(H+)= 2c(SO32��)+ c(HSO3��)+ c(OH��)
B��c(Na+)��c(HSO3��)��c(SO32��)��c(OH��)��c(H+)
C��c(Na+)��c(SO32��)��c(HSO3��)��c(OH��)��c(H+)
��3��������װ����ͨ�������SO2��Ϊ����֤A��SO2��Fe3+������������ԭ��Ӧ������ȡA�з�Ӧ�����Һ�ֳ����ݣ������������̽��ʵ�飬�������۲��������ǵ�̽�����̣���ѡ�Լ���KMnO4��Һ��KSCN��Һ��BaCl2��Һ��ϡ���ᡢϡ���ᡢϡ�� �ᡢBa(NO3)2��Һ�����Ƶ���ˮ��
|
��� |
ʵ�鷽�� |
ʵ������ |
���� |
|
������ |
����һ����Һ�м���KMnO4��Һ��Һ |
�Ϻ�ɫ��ȥ |
SO2��Fe3+��Ӧ������Fe2+ |
|
������ |
���ڶ�����Һ�м��� |
|
SO2��Fe3+��Ӧ������Fe2+ |
|
������ |
���ڶ�����Һ�м��� |
|
SO2��Fe3+��Ӧ������SO42�� |
���������ٵó��Ľ����Ƿ���� ��ԭ�� ��
���������Ƶķ������뷽���۾��������ҵõ���Ӧ���ۣ����㽫�������������
��4��װ��B���ܱ���Br���Ļ�ԭ������SO2�������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com