
【题目】(1)铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。

①某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种现象的原因,除了可能混有没反应完的磁性氧化铁外,还有一个原因是 ;
②若证明上述所得“铁块”中含有金属铝,可选择 (填试剂名称),所发生反应的离子方程式为 ;
(2)现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,
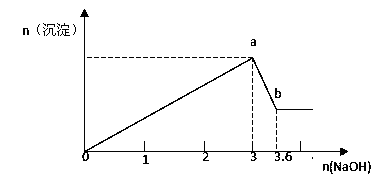
请计算出①a处沉淀的总物质的量 mol;
②c(FeCl3)= mol/L;③c(AlCl3)= mol/L
【答案】(1)①熔融的铁被空气中氧气氧化;②氢氧化钠溶液,2Al+2OH-+2H2O=2AlO![]() +3H2↑;(2)①1 ;②4;③6。
+3H2↑;(2)①1 ;②4;③6。
【解析】
试题分析:(1)①可能是熔融状态铁被空气中氧气氧化;②根据铝和铁都与酸发生反应,铝与氢氧化钠反应,产生氢气,但铁不与氢氧化钠反应,因此验证铝的可选择氢氧化钠,反应离子反应方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)①a~b段发生的反应是Al(OH)3 + OH- = AlO2- + 2H2O,根据铝元素守恒,n(AlCl3) = n[Al(OH)3] = n(NaOH) = (3.6-3)mol = 0.6mol,0~a发生反应离子反应方程式:Fe3 + + 3OH- = Fe(OH)3↓、Al3 + + 3OH- = Al(OH)3↓,Al3 + 消耗NaOH的物质的量为3×0.6mol = 1.8mol,则消耗n(Fe3 + ) = (3-1.8)/3mol = 0.4mol,n[Fe(OH)3] = 0.4mol,因此沉淀的总物质的量为(0.6 + 0.4) = 1mol;②根据①的计算,c(FeCl3) = 0.4/100×10-3mol·L-1 = 4mol·L-1;③c(AlCl3) = 0.6/100×10-3mol·L-1 = 6mol·L-1。


科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构和性质】 砷的一些化合物常用作半导体、除草剂、杀鼠药等,回答下列问题:
(1)写出基态砷原子的电子排布式_________________;有_________________个未成对电子。
(2)稼氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大到小的顺序是____________;
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为______________,1mol As4O6含有![]() 键的物质的量为____________mol。
键的物质的量为____________mol。

(4)As与N是同族元素,AsH3的沸点比NH3的沸点 ,原因是 。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,根据结构与性质的关系,H3AsO4的酸性比H3AsO3强的原因是: 。
(6)晶胞有两个基本要素
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子坐标参数A处Li为(0,0,1/2);B处As为(1/4,1/4,1/4);C处Li的坐标参数为 。
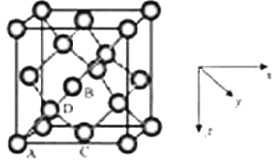
②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数,a=594pm,NA表示阿伏伽德罗常数的数值,其密度为 gcm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________反应(填“吸热”或“放热”),且m+n________p(填“>”、“=”或“<”)。
(2)减压使容器体积增大时,A的质量分数__________。(填“增大”、“减小”或“不变”,下同)
(3)若加入B(维持体积不变),则A的转化率____________。
(4)若升高温度,则平衡时B、C的浓度之比将____________。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
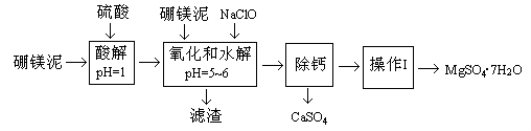
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有 。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有 。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式 。
在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为 。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法 。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 苯和甲苯互为同系物,都能使高锰酸钾褪色
B. 对二甲苯与氢气完全加成的产物的一氯代物有3种
C. 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
D. 淀粉、油脂、蛋白质的水解产物都是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~J是中学化学中常见的化学物质,它们之间的相互转化关系如下列框图所示(部分反应的产物未列出)。
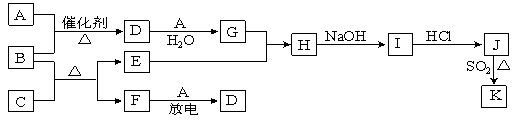
已知:A、F为无色气体单质,B为无色具有刺激性气味的碱性气体,C为黑色氧化物,E为红色金属单质。请回答下列问题:
(1)D的化学式为 ;F的电子式为 。
(2)B和C反应的化学方程式为 。该反应中生成1molF时,转移的电子数为 mol
(3)E与G的稀溶液反应的离子方程式为: 。
(4)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒精和醋酸是生活里的常用品,下列方法不能将二者鉴别开的是
A. 闻气味 B. 分别用来浸泡水壶中的水垢看是否溶解
C. 分别滴加NAOH溶液 D. 分别滴加石蕊试液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用冬青的提取物合成出一种抗结肠炎药物.其结构简式如图所示:

下列叙述中正确的是
A.该物质属于芳香族化合物.难溶于水
B.该物质可以发生加成、氧化、取代等反应
C.该物质能与强酸和强醎反应,但不能与碳酸氢钠反应
D.仅改变这三条侧链在苯环上的位置,还可得到10种同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com