
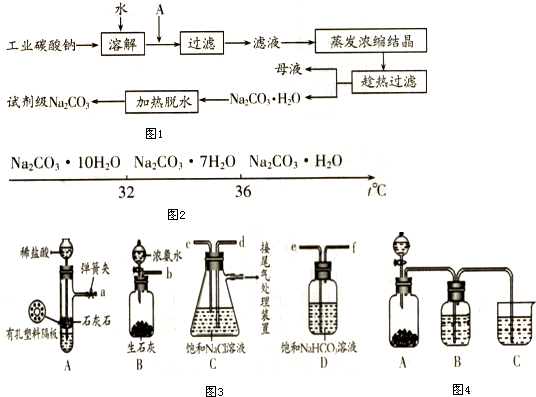
���� ��1����ҵ̼�����к���Mg2+��Fe3+��Ca2+�������ȼ�ˮ�ܽ���������Ƴ�������ȥ�����м��������NaOH��Һ��������Mg��OH��2��Fe��OH��3�������Ӷ���ȥ��þ���ӣ�������Һ��̼���ƺ��Ȼ��ƣ�������Ũ���ᾧ�����ȹ��ˣ��õ�һˮ̼���ƾ��壬�ټ�����ˮ�õ��Լ���̼���ƣ�
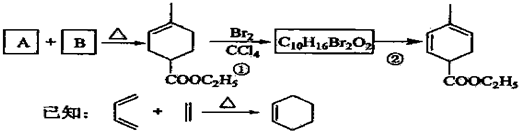
������������֪�Լ�A�dz���þ���Ӻ������ӵ��Լ�����ĸҺ���г��˺���Na+��CO32-��OH-�����⣬�����������ӣ���������ӣ�ʹ�����ľ���ΪNa2CO3•H2O����ֹ���¶ȹ��Ͷ�����Na2CO3•10H20�����Na2CO3•7H20���壬36����һ��ת�۵㣻
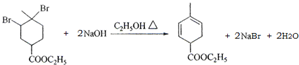
��a��HCl��BaCl2��AgNO3����˳���У������ӻ�����Ƿ������ʵ�飻
b��AgNO3��HNO3��Ba��NO3��2����˳�����ȼ���������̼������ӡ������ӡ���������Ӷ������������������������Ƿ������
c��HNO3��Ba��NO3��2��AgNO3���Լ��������̼���Ʒ�Ӧ���ټ������ᱵ�����Ƿ�����������ӣ��������������Һ�����Ƿ��������ӣ�
d��AgNO3��HCl��BaCl2����˳�����ȼ���������̼������ӡ������ӡ���������Ӷ������������������������������
��2��������CO2��ˮ�е��ܽ��С����������������ˮ�������ͨ�백����Ȼ����ͨ��CO2�����ڰ�����������ˮ��Ҫ��ֹ���������cͨ��NH3��dͨ��CO2��װ��A�Ʊ��Ķ�����̼�����к����Ȼ������壬��Ҫͨ������̼��������Һ��ȥ�������Ǽ���������Ҫϡ�������ն���İ���������̼��ˮ��Ӧ�γɲ��ȶ���̼�ᣬ��ʹˮ���ն�����̼�����٣����Ѷ�����̼ͨ�����а������ʼ��Ե�ˮ�У���ʹ���ɵ�̼���백ˮ������Ӧ�������������̼��������գ�
�����ɵ�NaHCO3����ӻ�����з�������IJ���Ϊ����ϴ�ӣ����ݹ���װ�÷����ش���Ҫ�IJ���������
�۱Ƚ�C��N��Si����Ԫ�صķǽ�����ǿ����������������ۺ����������ǿ���Ƚϣ�����ǿ�Ŀ����Ʊ���Ӧ�����������ģ���Һ©����Ϊ���ᣬA��Ϊ����ʯ�������̼��Ʒ�Ӧ���ɶ�����̼���������Դ���̼�ᣬΪ����ӷ���������ţ�������̼ͨ������̼��������Һ��ȥ�����������õ�������̼����ͨ���ձ��еĹ�������Һ�����ɹ����ɫ������֤��̼�����Դ��ڹ��
��� �⣺��1����ҵ̼�����к���Mg2+��Fe3+��Ca2�������ȼ�ˮ�ܽ���������Ƴ�������ȥ�����м��������NaOH��Һ��������Mg��OH��2��Fe��OH��3�������Ӷ���ȥ��þ���ӣ����Լ���NaOH��Һ�����ó�ȥ���л��е�Fe3+��Mg2+��
������������֪�Լ�A�dz���þ���Ӻ������ӵ��Լ�����ĸҺ���г��˺���Na+��CO32-��OH-�����⣬�����������ӣ���������ӣ�ʹ�����ľ���ΪNa2CO3•H2O����ֹ���¶ȹ��Ͷ�����Na2CO3•10H20�����Na2CO3•7H20���壬36����һ��ת�۵㣬���ȹ��������Na2CO3•10H20����ĺ�����
�ʴ�Ϊ������������Һ��Cl-��SO42-�����Na2CO3•10H20����ĺ�����
��a�����մ�˳������Լ�HCl��BaCl2��AgNO3�������ӻ�����Ƿ������ʵ�飬��a����
b�����մ�˳������Լ�AgNO3��HNO3��Ba��NO3��2��˳�����ȼ���������̼������ӡ������ӡ���������Ӷ������������������������Ƿ��������b����
c�����մ�˳������Լ�HNO3��Ba��NO3��2��AgNO3���ȼ��������̼���Ʒ�Ӧ���ټ������ᱵ�����Ƿ�����������ӣ��������������Һ�����Ƿ��������ӣ���c��ȷ��
d�����մ�˳������Լ�AgNO3��HCl��BaCl2��˳�����ȼ���������̼������ӡ������ӡ���������Ӷ��������������������������������d����
��2��������CO2��ˮ�е��ܽ��С����������������ˮ�������ͨ�백����Ȼ����ͨ��CO2�����ڰ�����������ˮ��Ҫ��ֹ���������cͨ��NH3��dͨ��CO2��װ��A�Ʊ��Ķ�����̼�����к����Ȼ������壬��Ҫͨ������̼��������Һ��ȥ��װ�������ӿڵ�����˳��Ϊ��aefd��cb��
��ͨ�백����������ˮ�γɳʼ��Եİ�ˮ���������̼��ˮ���ɵ�̼�ᷢ����Ӧ���������ڶ�����̼��������գ���ѡa��
�ʴ�Ϊ��efdc��a��
�����ɵ�NaHCO3����ӻ�����з�������IJ���Ϊ����ϴ�ӣ���������Ϊ�ձ�����������©����
�ʴ�Ϊ���ձ�����������©����
������ǿ�Ŀ����Ʊ���Ӧ�����������ģ�װ���е��Լ��ֱ�Ϊ����Һ©����Ϊ���ᣬA��Ϊ����ʯ�������̼��Ʒ�Ӧ���ɶ�����̼���������Դ���̼�ᣬΪ����ӷ���������ţ�������̼ͨ������̼��������Һ��ȥ������������˵��̼�ķǽ����Աȹ�ǿ��ʵ�������ǣ��õ�������̼����ͨ���ձ��еĹ�������Һ�����ɹ����ɫ��״������֤��̼�����Դ��ڹ��
�ʴ�Ϊ������̼��������Һ��C�г��ְ�ɫ��״������
���� ���⿼�������ʵķ����ᴿ�������Ʊ�ʵ�����̷����жϣ��������ʵ�����Ӧ�ã�����ʵ��������������ʵ��Ʊ�ԭ���ͼ��鷽���ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4 | B�� | PCl3 | C�� | SiCl4 | D�� | XeF4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | F-�Ľṹʾ��ͼ��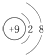 | B�� | CH4���ӵı���ģ�ͣ�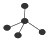 | ||
| C�� | CCl4�ĵ���ʽ��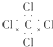 | D�� | ��ϩ�Ľṹ��ʽ��CH2CH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
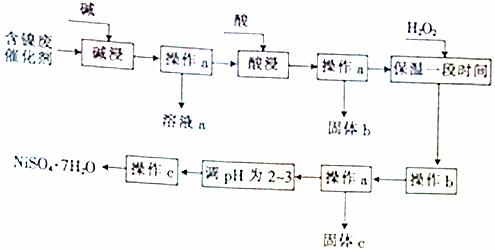
| ������ | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Al��OH��3 | 3.8 | 5.2 |
| Fe��OH��3 | 2.7 | 3.2 |
| Fe��OH��2 | 7.6 | 9.7 |
| Ni��OH��2 | 7.1 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ���ʹ�ϵ�ǣ�3�ԣ�NH3���T2�ԣ�H2O�� | |
| B�� | ����λʱ��������x mol NO��ͬʱ������x mol NH3����Ӧ�ﵽƽ��״̬ | |
| C�� | �ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ�������� | |
| D�� | �ﵽ��ѧƽ��ʱ��5������O2��=4������NO�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Լ��������ڷ����� | B�� | 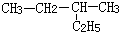 ��2-�һ����� ��2-�һ����� | ||
| C�� | 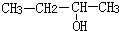 ��3-���� ��3-���� | D�� | 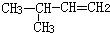 ��3-��-1-��ϩ ��3-��-1-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CaBr2 | B�� | Na2O2 | C�� | HBr | D�� | N2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com