
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和l00g 10.00%的K2SO4溶液.电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和l00g 10.00%的K2SO4溶液.电极均为石墨电极.分析 该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明C电极是电解池阴极,则d电极是阳极,连接电解池阳极的原电池电极是正极,则N为正极,M为负极;
(1)根据以上分析判断;电解氢氧化钠溶液时,阳极上氢氧根离子放电生成氧气;
(2)甲中电解氢氧化钠溶液即是电解水;乙中电解硫酸铜溶液生成硫酸;丙中电解硫酸钾溶液即是电解水;
(3)e电极上收集到气体在标准状况下体积为4.48L,e为阴极,其电极反应为2H++2e-=H2↑,b为阳极,其反应为4OH--4e-=O2↑+2H2O,电极c为阴极,电极反应为:2Cu2++2e-=Cu,根据转移电子守恒计算;
(4)电解硫酸铜溶液生成硫酸和氧气、Cu,根据溶液中减少的元素判断所加物质,结合电子守恒计算.
解答 解:该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明C电极是电解池阴极,则d电极是阳极,连接电解池阳极的原电池电极是正极,则N为正极,M为负极;
(1)根据以上分析N是原电池正极,电解氢氧化钠溶液时,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑,
故答案为:正;4OH--4e-=2H2O+O2↑;
(2)甲中电解氢氧化钠溶液即是电解水,水的量减少,溶液的体积减小,氢氧化钠的浓度增大,则pH变大;乙中电解硫酸铜溶液生成硫酸,溶液酸性增强,则pH减小;丙中电解硫酸钾溶液即是电解水,溶液显中性,pH不变;
故答案为:增大;减小;不变;
(3)e电极上收集到气体在标准状况下体积为4.48L,e为阴极,其电极反应为2H++2e-=H2↑,生成4.48L氢气,其的物质的量为0.2mol,则转移电子为0.4mol,b为阳极,其反应为4OH--4e-=O2↑+2H2O,由电子守恒可知,生成氧气为0.1mol,其体积为2.24L;电极c为阴极,电极反应为:2Cu2++2e-=Cu,由电子守恒可知,生成Cu为0.2mol,其质量为12.8g;
故答案为:2.24L;12.8;
(4)电解硫酸铜溶液生成硫酸和氧气、Cu,其电解方程式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;溶液中减少的元素为Cu和O元素,所以要是电解质溶液复原需加CuO,转移电子为0.4mol,则CuO为0.2mol,其质量为16g;
故答案为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;CuO;16.
点评 本题考查了电解池原理的应用,注意根据电解池电极上发生的现象来判断阴阳极和原电池的正负极,再结合电子守恒分析解答,题目难度中等,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 脱落酸 | B. | 乙烯 | C. | 生长素 | D. | 甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,11.2升CCl4中含有氯原子的数目为2 NA | |
| B. | 500mL 0.5mol/L的Na2CO3溶液中,含有CO32-的数目小于0.25NA | |
| C. | 常温下电解NaNO3溶液,当阳极产生气体22.4升时,转移电子的数目为4NA | |
| D. | 将0.1 mol N2和0.3 mol H2置于密闭容中充分反应,可得0.2NA个NH3分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
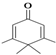 如图所示的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来命名为Penguinone.下列有关Penguinone的说法不正确的是( )
如图所示的分子酷似企鹅,化学家Chris Scotton将该分子以企鹅来命名为Penguinone.下列有关Penguinone的说法不正确的是( )| A. | Penguinone中存在两种官能团 | |
| B. | Penguinone是一种芳香醛 | |
| C. | Penguinone中存在与乙烯相同的官能团,所以其与乙烯有相似的性质 | |
| D. | 如果该分子中的双键都能加成,则1 mol Penguinone能与3 mol氢气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 分子代号 | 甲 | 乙 | 丙 | 丁 |
| 电子数 | 10 | 16 | 18 | 26 |
| A. | 四种气体中至少有两种气体分子互为同分异构体 | |
| B. | 四种气体通入溴的四氯化碳溶液中,都能使其褪色 | |
| C. | 气体乙的分子内所有的原子在同一平面上 | |
| D. | 鉴别丙和丁两种气体,可以用高锰酸钾酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O、BaSO4、O2 | B. | FeCl2 溶液、Fe 粉、Cl2 | ||
| C. | H2O、CaCO3、SO3气体 | D. | H2O、SiO2、HCl 气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-个数多于CO32-个数 | |
| B. | 逐滴加入稀盐酸,刚开始会产生气体 | |
| C. | c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| D. | 2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
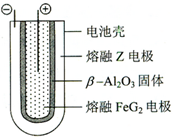 X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.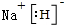 ;五种元素中非金属气态氢化物还原性最强的是H2S(写化学式).
;五种元素中非金属气态氢化物还原性最强的是H2S(写化学式). Fe+2ZG放电时,电池的正极反应式为Fe2++2e-=Fe:充电时,钠(写物质名称)电极接电源的负极.
Fe+2ZG放电时,电池的正极反应式为Fe2++2e-=Fe:充电时,钠(写物质名称)电极接电源的负极.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) | |
| B. | 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| C. | 含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)=c(HCO${\;}_{3}^{-}$) | |
| D. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com