
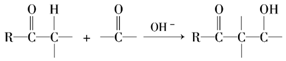 .
. ,则异蒲勒醇的结构简式为
,则异蒲勒醇的结构简式为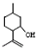 .
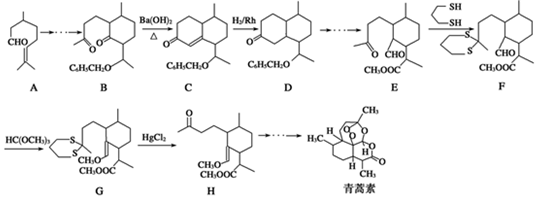
.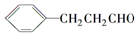 )的合成路线流程图(无机试剂任选).
)的合成路线流程图(无机试剂任选). 分析 (1)根据E的结构判断含有的官能团;
(2)由E→F的结构可知,羰基中C=O双键变成C-S单键,由G→H的结构可知C-S单键又变成羰基,目的是保护羰基;
(3)由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α-H与C=O先发生发生加成反应,再发生消去反应生成C;
(4)由最终分子的结合,结合异蒲勒醇分子有3个手性碳原子、与A互为同分异构体,可知其结构为环状,分子内脱水,应含有-OH,根据A的结合可知-OH处于环中甲基的间位位置,结合加成产物应是与氢气发生1,4-加成,据此书写;
(5)结合流程中B→C→D的变化分析设计,乙烯在催化剂加热条件下与水反应生成乙醇,乙醇催化氧化生成乙醛,乙醛与苯甲醛在氢氧化钡条件下生成 ,在氢气/Rh条件下发生加成反应生成
,在氢气/Rh条件下发生加成反应生成 .
.
解答 解:(1)根据E的结构可知,含有的含氧官能团为酯基、醛基、羰基,
故答案为:酯基、羰基;
(2)由E→F的结构可知,羰基中C=O双键变成C-S单键,由G→H的结构可知C-S单键又变成羰基,目的是保护羰基,
故答案为:保护羰基;
(3)由题目信息可知,结合B、C的结构可知,C=O双键变成C=C双键,应是B中连接羰基的甲基上的α-H与C=O先发生发生加成反应产生C-OH,再发生消去反应生成产生C=C双键生成C,
故答案为:加成反应、消去反应;
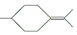
(4)由最终分子的结合,结合异蒲勒醇分子有3个手性碳原子、与A互为同分异构体,可知其结构为环状,分子内脱水,应含有-OH,根据A的结合可知-OH处于环中甲基的间位位置,结合加成产物 可知应是异蒲勒醇与氢气发生1,4-加成,则异蒲勒醇的结构简式为:
可知应是异蒲勒醇与氢气发生1,4-加成,则异蒲勒醇的结构简式为: ,
,
故答案为: ;
;
(5)结合流程中B→C→D的变化分析设计,乙烯在催化剂加热条件下与水反应生成乙醇,乙醇催化氧化生成乙醛,乙醛与苯甲醛在氢氧化钡条件下生成 ,在氢气/Rh条件下发生加成反应生成
,在氢气/Rh条件下发生加成反应生成 ,
,
工艺流程图为: ,
,
故答案为: .
.
点评 本题考查了有机物推断与合成,涉及对工艺流程的分析与推断、有机反应类型、官能团、合成工艺流程的设计,难度中等,注意根据转化关系中有机物的结构理解发生的反应,(5)中方案设计,注意利用题目中合成路线中增长碳链的信息设计,为热点题型.


 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
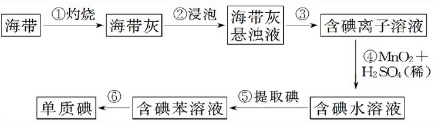
| 密度(g/cm3) | 熔点(.C) | 沸点(.C) | |
| 碘 | 4.93 | 113.5 | 184.35 |
| 苯 | 0.885 | 80.10 | 5.53 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
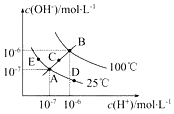 已知水的电离平衡曲线如图示,试回答下列问题:
已知水的电离平衡曲线如图示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、Na+、K+ | B. | SO42-、Cl-、K+ | C. | Cl-、NO3-、K+ | D. | HCO3-、SO42-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
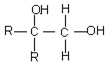 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$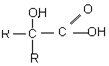

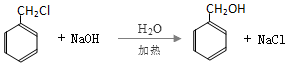 ;
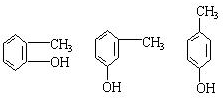
;
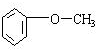
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸氢钠与盐酸反应:CO3-+2H+═H2O+CO2↑ | |
| C. | 醋酸溶液与氢氧化钠溶液反应:CH3COOH+OH-═CH3COO-+H2O | |
| D. | 金属铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com