
A.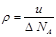 | B.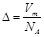 | C.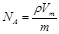 | D.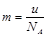 |
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.0.3 mol/L | B.0.4 mol/L | C.0.5 mol/L | D.0.6 mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等物质的量的N2和CO所含分子数均为NA |
| B.标准状况下,11.2 L氟化氢所含的分子数为0.5NA |
| C.常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.5NA |
| D.常温常压下,14.9g KCl与NaClO的混合物中含氯元素的质量为7.1g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁制品上电镀锌时,阴极质量每增加65g时转移的电子数是2NA |
| B.5.6L Cl2与足量铁粉反应时转移的电子数为0.5NA |
| C.1L 1mol·L-1的CH3COOH溶液中含有H+的数目是NA |
| D.1L 0.5mol·L-1的Na2CO3溶液中含有CO32-的数目是0.5NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0 g | 75.0 g | 140.0 g |
| 反应后 | 37.0 g | 79.0 g | 140.5 g |

 Na2S + 4CO↑ ②Na2SO4 + 4CO
Na2S + 4CO↑ ②Na2SO4 + 4CO Na2S + 4CO2
Na2S + 4CO2 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.14N的质量数 | B.氕原子的相对质量 |
| C.氯元素的相对原子质量 | D.氟化钠的摩尔质量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2Na2O 2Na2O +O2
2Na2O 2Na2O +O2 2Na2O2 。
2Na2O2 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol苯含有的C=C键数为3NA |
| B.1mol Na2O2与水完全反应时转移的电子数为NA |
| C.含NA个Na+的Na2O溶解于1L水中,Na+浓度为1mol·L-1 |
| D.1mol O2和2mol SO2在密闭容器中充分反应后的分子数等于2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com