
������,������Ⱦ��Ϊ����,���������������ü�����⡣
(1)���������һ�������ȼҵ��Ʒ������������������ķ���,��������:
(��)����SO2�ķ���ͨ���ⱥ��ʳ��ˮ�����õ�����Һ��,��NaHSO3��Һ��
(��)����ⱥ��ʳ��ˮ�������巴Ӧ���Ƶ����ᡣ
(��)���������NaHSO3��Һ��,��Ӧ���õ���SO2�������,���ɵ�NaClѭ�����á�
��д������(��)��Ӧ�Ļ�ѧ����ʽ: �� ������������������������������;
��д������(��)�е�ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ: �� ������������������;
��д������(��)��Ӧ�����ӷ���ʽ: ����������������������������������
(2)����ѧ���������Fe2+��Fe3+�����ӵĴ�����,�����½�SO2������S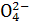 ��ʵ��SO2�Ļ������á�ij�о���ѧϰС��ݴ���������·���,��ʵ���������²ⶨת������SO2������S
��ʵ��SO2�Ļ������á�ij�о���ѧϰС��ݴ���������·���,��ʵ���������²ⶨת������SO2������S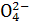 ��ת���ʡ�
��ת���ʡ�
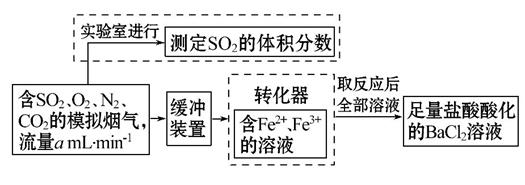
�ٸ�С�������ͼװ����ʵ���Ҳⶨģ��������SO2���������,X��Һ��������������������(��д���)
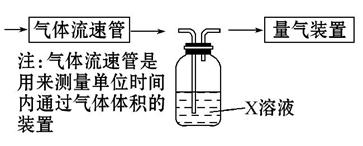
A.��ĵ�����Һ B.���Ը��������Һ
C.����������Һ D.�Ȼ�����Һ
��������ʵ�����ڱ�״���½��е�,���ⶨת������SO2������S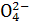 ��ת����,��֪��������,����ⶨ������������������������������������
��ת����,��֪��������,����ⶨ������������������������������������
�����������SO2�ڻ�����е��������,��Ҫ���������,һ����SO2�����,һ���ǻ���������������������װ��,���������SO2�����������;����ϴ��ƿ�е�X��Һ,�����ܹ����SO2����������Զ���ϴ��ƿ�е���Һ,��������SO2��Ӧ,���ܷ������Ե���ɫ�仯,�Ա�ȷ����Ӧ���յ㡣���SO2��ת����,Ӧ���SO2���������������S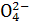 ��������Ϊ��ǰһ���������SO2�ڻ�����еĺ���,����ֻ��ȷ�����������������������������,ֻ�����ͨ��ʱ�䡣Ҫ��SO2��ת����,ֻ��ȷ������������
��������Ϊ��ǰһ���������SO2�ڻ�����еĺ���,����ֻ��ȷ�����������������������������,ֻ�����ͨ��ʱ�䡣Ҫ��SO2��ת����,ֻ��ȷ������������
��:(1)��SO2+NaOH====NaHSO3
��2NaCl+2H2O 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
��HS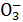 +H+====SO2��+H2O
+H+====SO2��+H2O
(2)��A��B ��ʵ��ʱ�� ���������ữ��BaCl2��Һ�����ɳ���������


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ������Fe��FeO��Fe2O3�Ļ�����м���120 mL 4 mol/L��ϡ����,ǡ��ʹ�������ȫ�ܽ�,�ų�1.344 L NO(��״��),��������Һ�м���KSCN��Һ,��ɫ���֡�����������CO�ڼ����»�ԭ��ͬ�����Ļ����,���յõ��������ʵ���Ϊ
A. 0.21 mol B. 0.24 mol C. 0.16 mol D. 0.14 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8 g Na2O2��Na2O��Na2CO3��NaOH�Ļ������200 g��������Ϊ3.65%������ǡ�÷�Ӧ,������Һ,���յù�������Ϊ��(����)
A.8 g���� B.15.5 g���� C.11.7 g�� ��D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ����������Ϊԭ����������������β���к���SO2,Ϊ���ڼ��,ʵʩ��������,�����ʺϲⶨ����β��SO2�������Լ���(����)
A.Ʒ����Һ B.Ũ����
C.��ˮ��������Һ D.���϶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵���д������(����)
A.Na2SO3��BaCl2��Һ����,�а�ɫ��������,��������������ʧ
B.��SO2����ͨ��Ba(OH)2��Һ���а�ɫ��������
C.��SO2����ͨ��BaCl2��Һ���а�ɫ��������
D.��SO2����ͨ�������ữ��BaCl2��Һ���а�ɫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ����(����)
A.ʵ�������Ȼ�狀���ʯ���ư�:
N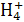 +OH-
+OH-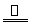 NH3��+H2O
NH3��+H2O
B.NaOH��Һ��NH4Cl��Һ��ϼ���:
N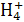 +OH-
+OH- NH3��H2O
NH3��H2O
C.��ˮ�м�����:NH3��H2O+H+====N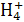 +H2O
+H2O
D.��ˮ��ͨ������CO2:
CO2+NH3��H2O====N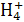 +HC
+HC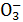 +H2O
+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪:A��BΪ�����ķǽ��������Ҿ�Ϊ����;�ס���Ϊ��������,����I��Ũ��Һ�з����ۻ�;C��H��J����Һ���ʼ��ԡ������ʼ��ת����ϵ����(����������δ����,��δע����Ӧ����):
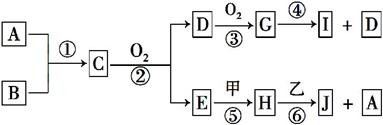
(1)д����Ӧ�ڵĻ�ѧ����ʽ�� ��
(2)��Ӧ����ÿ����1 mol G,ת�Ƶ��ӵ����ʵ���Ϊ������ ����
(3)��Ӧ�����ӷ���ʽ���� ��
(4)ʵ�����б���I�ķ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ס�����Ԫ�����ڱ���ͬһ���������Ԫ�أ�����ԭ������Ϊx�����ҵ�ԭ��������������( )
A��x+2 B��x+4 C��x+8 D��x+18
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������H��һ�����ϣ������ڽ����У���������·�ߺϳɣ�
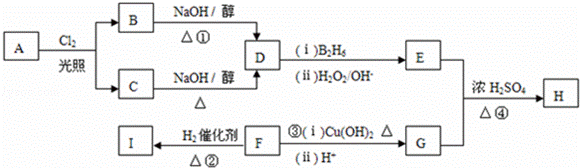
��֪��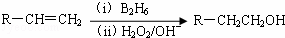 ��B2H6Ϊ�����飩
��B2H6Ϊ�����飩
�ش��������⣺
��1��0.1mol��A�������г��ȼ�տ��Բ���8.96L CO2����״���£���9.0g H2O��A�ķ���ʽ��������
��2����Ӧ�ٺܵ͢ķ�Ӧ��������������
��3��B��C��Ϊһ�ȴ�����B�ĺ˴Ź���������ʾֻ��һ�ֻ�ѧ��������ԭ�ӣ���B�Ľṹ��ʽΪ������D��ϵͳ����������Ϊ������
��4���ڴ���������1mol F��2mol H2��Ӧ������I�� ����F�Ľṹ��ʽ��������
����F�Ľṹ��ʽ��������
��5����Ӧ�ۣ�ⅰ���Ļ�ѧ����ʽΪ��������Ӧ�ܵĻ�ѧ����ʽΪ������
��6��д��������G������ͬ�����ŵ�G�ķ�����ͬ���칹��Ľṹ��ʽ��������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com