
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
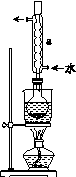
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________。检验是否存在该杂质的方法是____________________________。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:________________________________________________________________________
________________________________________________________________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O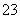 +I2===S4O
+I2===S4O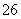 +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
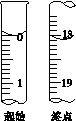
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO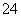 ,常用作脱氯剂,该反应的离子方程式为____________________________________________。
,常用作脱氯剂,该反应的离子方程式为____________________________________________。
(1)使硫粉易于分散到溶液中
(2)冷凝管 冷凝回流
(3)Na2SO4 取少量产品溶于过量盐酸,过滤,向滤液中加BaCl2溶液,若有白色沉淀,则产品中含有Na2SO4
(4)S2O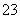 +2H+===S↓+SO2↑+H2O
+2H+===S↓+SO2↑+H2O
(5)由无色变蓝色
(6)18.10 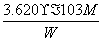 ×100%
×100%
(7)S2O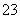 +4Cl2+5H2O===2SO
+4Cl2+5H2O===2SO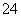 +8Cl-+10H+
+8Cl-+10H+
[解析] (1)硫粉难溶于水,微溶于乙醇,故硫粉用乙醇润湿后易扩散到溶液中。(2)装置中仪器a是冷凝管,起冷凝回流汽化的反应物的作用。(3)因反应物Na2SO3易被空气中的氧气氧化成Na2SO4,故可能存在的无机杂质是Na2SO4;检验产品中是否含有Na2SO4,即检验SO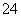 是否存在,需要防止SO
是否存在,需要防止SO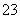 的干扰,故不能用具有强氧化性的硝酸酸化,而应用盐酸酸化,过滤除去不溶物,再向滤液中滴加氯化钡溶液。(4)产品发黄,说明产品中含有硫杂质,这是由于在酸性环境中Na2S2O3不稳定,发生歧化反应:2H++S2O
的干扰,故不能用具有强氧化性的硝酸酸化,而应用盐酸酸化,过滤除去不溶物,再向滤液中滴加氯化钡溶液。(4)产品发黄,说明产品中含有硫杂质,这是由于在酸性环境中Na2S2O3不稳定,发生歧化反应:2H++S2O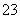 ===S↓+SO2↑+H2O所致。(5)滴定终点时,过量的单质碘使无色的淀粉溶液变蓝,可指示滴定终点。(6)起始读数为0.00 mL,终点读数为18.10 mL,所以消耗碘的标准溶液的体积为18.10 mL-0.00 mL=18.10 mL;根据2Na2S2O3·5H2O~2S2O
===S↓+SO2↑+H2O所致。(5)滴定终点时,过量的单质碘使无色的淀粉溶液变蓝,可指示滴定终点。(6)起始读数为0.00 mL,终点读数为18.10 mL,所以消耗碘的标准溶液的体积为18.10 mL-0.00 mL=18.10 mL;根据2Na2S2O3·5H2O~2S2O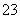 ~I2,得n(Na2S2O3·5H2O) =2n(I2)=2×0.100 0 mol·L-1×18.10×10-3 L=3.620×10-3 mol,则产品的纯度
~I2,得n(Na2S2O3·5H2O) =2n(I2)=2×0.100 0 mol·L-1×18.10×10-3 L=3.620×10-3 mol,则产品的纯度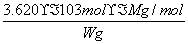 ×100%=
×100%=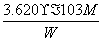 ×100%。(7)S2O
×100%。(7)S2O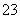 被Cl2氧化成SO
被Cl2氧化成SO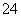 ,Cl2被还原为Cl-,首先根据化合价升降总数相等写出S2O
,Cl2被还原为Cl-,首先根据化合价升降总数相等写出S2O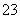 +4Cl2→2SO
+4Cl2→2SO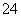 +8Cl-,然后根据原子守恒和电荷守恒写出S2O
+8Cl-,然后根据原子守恒和电荷守恒写出S2O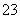 +4Cl2+5H2O===2SO
+4Cl2+5H2O===2SO +8Cl-+10OH-。
+8Cl-+10OH-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
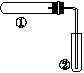
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )
| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2 的混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同
B.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸
C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
D.用AgNO3溶液可以鉴别KCl和KI
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
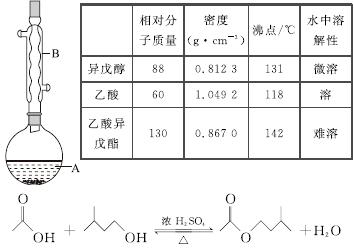
实验步骤:
在A中加入4.4 g异戊醇、6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50 min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是________________。
(2)在洗涤操作中,第一次水洗的主要目的是____________________________________,第二次水洗的主要目的是________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是___________________________________________。
(5)实验中加入少量无水MgSO4的目的是________。
(6)在蒸馏操作中,仪器选择及安装都正确的是________(填标号)。

a. b.
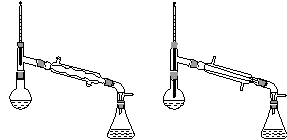
c. d.
(7)本实验的产率是________(填标号)。
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏__________(填“高”或“低”),其原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验 。
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。

氨的测定装置(已省略加热和夹持装置)
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是__________________________________________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用________式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将________(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是____________________;滴定终点时,若溶液中c(Ag+)=2.0×10-5 mol·L-1,c(CrO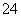 )为________mol·L-1。[已知:Ksp(Ag2CrO4)=1.12×10-12]
)为________mol·L-1。[已知:Ksp(Ag2CrO4)=1.12×10-12]
(6)经测定,样品X中钴、氨和氯的物质的量之比为1∶6∶3,钴的化合价为________,制备X的化学方程式为______________________________________;X的制备过程中温度不能过高的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
2014年2月,我国中东部地区遭遇严重的雾霾天气,京津冀地区的空气污染级别高达6级,PM2.5值逼近1000(“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物).下列有关环境污染与防护的说法正确的是 ( )
A.CO,、NO、NO2都是大气污染气体,在空气中能稳定存在
B.使用清洁能源是防止酸雨发生的重要措施之一
C.PM2.5属于胶体,可以通过静电除尘装置除去
D.治理汽车尾气中的CO和NO2,可以通过催化转化装置,转化成无毒的C02和NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
观察是研究物质性质的一种基本方法.一同学将一小块金属钠露置于空气中,观察到下列现象:银白色→①变灰暗→②变白色→③出现液滴→④白色固体,下列说法中正确的是 ( )
A.①发生了氧化还原反应
B.②变白色是因为生成了碳酸钠
C.③是碳酸钠吸收空气中的水蒸气形成了溶液
D.④只发生物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
按以下实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
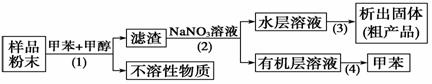
下列说法错误的是 ( )
A.步骤(1)需要过滤装置
B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚
D.步骤(4)需要蒸馏装置
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com