
实验室用NaOH固体配制480mL 1.0mol/L的NaOH溶液,请回答下列问题:
(1)应称取NaOH固体的质量 g
(2)实验仪器除了托盘天平、药匙、烧杯、玻璃棒外,还应有
(3)容量瓶上需标有以下五项中的 (序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)使用容量瓶前必须进行的一步操作是 .
(5)配制时,其正确的操作顺序是
A、用30mL水洗涤烧杯2﹣3次,洗涤液均转入容量瓶,振荡
B、用托盘天平准确称取所需质量的NaOH,放入烧杯,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入500mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切
F、继续往容量瓶内小心加水,直到液面接近刻度线1﹣2cm处
(6)下列配制的溶液浓度偏大的是
A、NaOH在烧杯中溶解后,未冷却就转移到容量瓶中
B、向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
C、未洗涤溶解NaOH的烧杯
D、定容时俯视刻度线.
考点:
配制一定物质的量浓度的溶液.
专题:
实验题.
分析:
(1)根据m=CVM计算溶质的质量;
(2)根据配制溶液的操作步骤选择所用仪器,进而判断缺少的仪器;
(3)容量瓶上需标有温度、容量、刻度线;
(4)溶液配制最后需要反复上下颠倒摇匀,故使用容量瓶之前需要检查容量瓶是否漏水;
(5)根据配制溶液的操作步骤,进行操作步骤排序;
(6)分析操作对溶质的物质的量或对溶液的体积的影响,根据c= 分析对溶液浓度的影响.
分析对溶液浓度的影响.
解答:
解答:解:(1)m=CVM=1mol/L×0.5L×40g/mol=20g,故答案为:20g;
(2)溶液配制过程中,用烧杯溶解烧碱,用玻璃棒搅拌和引流,用500mL的容量瓶配制溶液,用胶头滴管定容,用托盘天平称量烧碱,用药匙取药品,实验仪器除了托盘天平、药匙、烧杯、玻璃棒外,还应有500mL容量瓶、胶头滴管,故答案为:500mL容量瓶、胶头滴管;
(3)容量瓶上需标有温度、容量、刻度线,故答案为:①③⑤;
(4)溶液配制最后需要反复上下颠倒摇匀,故使用容量瓶之前需要检查容量瓶是否漏水,
故答案为:检查容量瓶是否漏水;
(5)配制溶液的步骤是:称量、溶解、冷却、转移、洗涤、转移、定容、摇匀,所以其排序是BCAFED,
故答案为:BCAFED;
(6)A.NaOH溶解时放出大量的热,未冷却立即配制溶液,导致溶液的体积偏小,则配制溶液的浓度偏高;
B.向容量瓶中转移溶液时不慎洒出,导致溶质的物质的量偏小,则配制溶液的浓度偏低;
C.溶解NaOH固体之后的烧杯未洗涤,导致溶质的物质的量偏小,则配制溶液的浓度偏低;
D.定容时俯视刻度线,导致溶液的体积偏小,则配制溶液的浓度偏高;
故选AD.
点评:
本题考查了一定物质的量浓度溶液的配制,难度不大,注意计算氢氧化钠的质量时,V应该是500mL而不是480mL,为易错点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
化合物A有稳定性好、抗氧化能力强的特点,其结构如图 .分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(
.分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(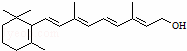 )和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
)和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
完成下列填空:
(1)化合物B能发生下列哪种类型的反应
a.取代反应b.加成反应c.缩聚反应d.氧化反应
(2)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含五元环).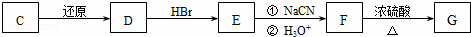
已知:ROOH RCH2OH RX
RCH2OH RX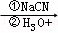 RCOOH
RCOOH
化合物C的结构简式为 .
(3)反应F→G的化学方程式为
(4)化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式、、.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在25℃、101kPa的条件下,同质量的CH4和A气体的体积之比是11:4,则A的摩尔质量为 .
在V L Al2(SO4)3溶液中,测得含Al3+的质量为a g,则Al2(SO4)3溶液的物质的量浓度为 mol/L,SO42﹣的物质的量浓度为 mol/L.
(3)将5.3gNa2CO3溶于水配成1L溶液,要使Na+浓度变为0.2mol/L,需要加入NaCl固体 g
(4)实验测得CO和O2混合气体的密度是氢气的15.5倍,其中氧气的体积分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子的检验方法中正确的是( )
|
| A. | 某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl﹣ |
|
| B. | 某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42﹣ |
|
| C. | 某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ |
|
| D. | 某溶液加KOH溶液生成红褐色沉淀,说明原溶液中有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中物质的量浓度为1mol/L的是( )
|
| A. | 将40g NaOH溶解在1L水中 |
|
| B. | 将22.4L HCl气体溶于水配成1L溶液 |
|
| C. | 从1L 2mol/L的H2SO4溶液中取出0.5L |
|
| D. | 将10g NaOH溶解在少量水中,再加蒸馏水至溶液体积为250mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒用作引流的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
|
| A. | ①和② | B. | ①和③ | C. | ③和④ | D. | ①和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 摩尔是6.02×1023个结构微粒的集体 |
|
| B. | 0.012kg12C所含的原子数精确值是6.02×1023 |
|
| C. | 1molH就是1mol氢 |
|
| D. | 1molH2SO4的质量是98g |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用NaOH固体配制480mL 1.0mol/L的NaOH溶液,请回答下列问题:
(1)应称取NaOH固体的质量 g
(2)实验仪器除了托盘天平、药匙、烧杯、玻璃棒外,还应有
(3)容量瓶上需标有以下五项中的 (序号)
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)使用容量瓶前必须进行的一步操作是 .
(5)配制时,其正确的操作顺序是
A、用30mL水洗涤烧杯2﹣3次,洗涤液均转入容量瓶,振荡
B、用托盘天平准确称取所需质量的NaOH,放入烧杯,加入少量水(约30mL),用玻璃棒慢慢搅拌,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入500mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切
F、继续往容量瓶内小心加水,直到液面接近刻度线1﹣2cm处
(6)下列配制的溶液浓度偏大的是
A、NaOH在烧杯中溶解后,未冷却就转移到容量瓶中
B、向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
C、未洗涤溶解NaOH的烧杯
D、定容时俯视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的性质随着元素原子序数的递增而呈周期性变化的原因是( )
|
| A. | 元素原子的核外电子排布呈周期性变化 |
|
| B. | 元素的原子半径呈周期性变化 |
|
| C. | 元素的化合价呈周期性变化 |
|
| D. | 元素的金属性、非金属性呈周期性变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com