
【题目】铝是一种重要金属,从铝土矿(主要成分为Al2O3 , Fe2O3、SiO2等)中冶炼Al的工业生产流程如下图: 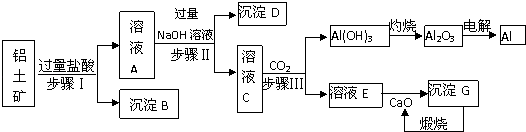
(1)溶液A中含的阳离子主要有 .
(2)写出步骤II生成溶液C 的离子方程式 ,
步骤I、II、III都要用到的分离方法是 .
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有(填化学式).
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
.
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)(用含a、b的最简式表示).
【答案】
(1)Al3+、Fe3+、H+
(2)Al3++4OH﹣=AlO2﹣+2H2O;过滤
(3)CO2、NaOH
(4)2Al+Fe2O3 ![]() Al2O3+2Fe
Al2O3+2Fe
(5)![]() ×100%
×100%
【解析】解:由工艺流程可知,铝土矿(主要成分为Al2O3 , Fe2O3、SiO2等),铝土矿与过量的盐酸反应得沉淀B和溶液A,则固体B为SiO2 , 过滤得滤液A含有氯化铝、氯化铁、盐酸等,滤液中加入过量的NaOH,可推知沉淀D为氢氧化铁,过滤得滤液C含有偏铝酸钠、氯化钠,所以向滤液C中通入二氧化碳,生成氢氧化铝沉淀与溶液E为碳酸氢钠或碳酸钠溶液,过滤后向E溶液中加入氧化钙得沉淀G为碳酸钙,同时得到氢氧化钠溶液,氢氧化钠溶液可以循环利用,碳酸钙煅烧分解得氧化钙和二氧化碳都可以循环利用,Al(OH)3灼烧得氧化铝,电解熔融的氧化铝可得铝。
(1.)由上述分析可知溶液A中含的阳离子主要有 Al3+、Fe3+、H+ ,
所以答案是:Al3+、Fe3+、H+;
(2.)步骤II过量的氢氧化钠与氯化铝反应生成偏铝酸钠,反应的离子方程式为Al3++4OH﹣=AlO2﹣+2H2O,根据上面的分析可知,步骤I、Ⅱ、Ⅲ都要用到的分离方法是 过滤,所以答案是:Al3++4OH﹣=AlO2﹣+2H2O;过滤;
(3.)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有CO2、NaOH,所以答案是:CO2、NaOH;
(4.)铝与氧化铁发生反应的化学方程式为2Al+Fe2O3 ![]() Al2O3+2Fe,所以答案是:2Al+Fe2O3
Al2O3+2Fe,所以答案是:2Al+Fe2O3 ![]() Al2O3+2Fe;
Al2O3+2Fe;
(5.)a吨铝土矿可以冶炼出b吨的铝,则由铝元素守恒可知,需要纯氧化铝的质量为 ![]() b吨,所以原铝土矿中Al2O3的纯度为
b吨,所以原铝土矿中Al2O3的纯度为 ![]() ×100%=
×100%= ![]() ×100%,所以答案是:
×100%,所以答案是: ![]() ×100%.
×100%.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
【题目】图I是NO2(g)+CO(g)![]() CO2(g)+N0(g)反应过程中能量变化示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X增大的变化关系曲线如图II所示。下列有关说法正确的是
CO2(g)+N0(g)反应过程中能量变化示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X增大的变化关系曲线如图II所示。下列有关说法正确的是
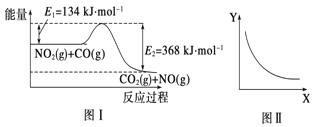
A. 该反应的焓变 △H=+234kJ/mol
B. 若X表示温度,则Y表示的可能是CO2的物质的量浓度
C. 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
D. 若X表示反应时间,则Y表示的可能是混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷分子是以碳原子为中心的正四面体结构而不是正方形的平面结构,其理由是
A. CHCl3只有一种结构
B. CH2Cl2只有一种结构
C. CH4分子受热分解
D. CH4的四个价键的长度和强度都相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体和溶液的说法中,正确的是
A. 胶体和溶液均能导电
B. 胶体和溶液的本质区别是能否产生丁达尔效应
C. 明矾水解生成Al(OH)3胶体,可用作净水剂
D. 布朗运动是胶体粒子特有的运动方式,可以据此区分胶体与溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO和O2转化为NO2的反应机理如下:
①2NO(g)![]() N2O2(g)(快) △H1<0 平衡常数 K1
N2O2(g)(快) △H1<0 平衡常数 K1
②N2O2(g)+O2(g) ![]() 2NO2化) (慢) △H2<0 平衡常数K2
2NO2化) (慢) △H2<0 平衡常数K2
下列说法正确的是
A. 2NO(g) +O2(g)![]() 2NO2(g)的△H= -(△H1+△H2)
2NO2(g)的△H= -(△H1+△H2)
B. 2NO(g) +O2(g)![]() 2NO2 (g)的平衡常数 K =
2NO2 (g)的平衡常数 K =![]()
C. 反应②的速率大小决定2NO(g)+O2(g) ![]() 2NO2(g)的反应速率
2NO2(g)的反应速率
D. 反应过程中的能量变化可用下图表示

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组模拟“人工树叶”电化学装置如图所示,该装置能将H2O和CO2转化为糖类(C6H12O6)和O2,X、Y是特殊催化剂型电极,已知:装置的电流效率等于生成产品所需的电子数与电路中通过总电子数之比。下列说法错误的是( )
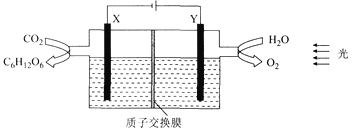
A. 该装置中Y电极发生氧化反应
B. X电极的电极反应式为 6CO2+24H++24e-=== C6H12O6+6H2O
C. 理论上,每生成22.4 L(标准状况下)O2,必有4 mol H+由X极区向Y极区迁移
D. 当电路中通过3 mol e时,生成18 g C6H12O6,则该装置的电流效率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①﹣⑨在表中的位置,用化学用语回答下列问题:
族 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)写出⑧的原子结构示意图 .
(2)④、⑤、⑥的原子半径由大到小的顺序为(用元素符号回答).
(3)②、③、⑦的最高价含氧酸的酸性由强到弱顺序是(用化学式回答)
(4)③元素所形成单质的结构式为 .
(5)⑥的单质与①、⑨两种元素形成化合物的水溶液反应的离子方程式为: .
(6)⑤元素与⑨元素形成的化合物中,化学键类型为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与电化学腐蚀无关的是( )
A. 光亮的自行车钢圈不易生锈
B. 黄铜(Cu-Zn合金)制的铜锣不易产生铜绿
C. 铜铝电线一般不连接起来作导线
D. 镀锡的铁皮,破损后铁皮反而易被腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com