
(10分)下表是元素周期表的一部分,A、B、C、D、E、X是下表中给出元素组成的常见单质或化合物。
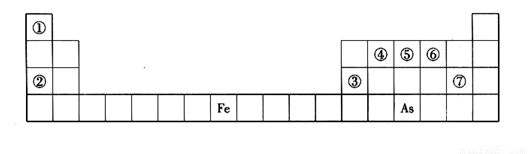
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
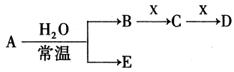
(1)若E为单质气体,D为白色沉淀,A的化学式可能是 , C与X反应的离子方程式为 。
(2)若E为氧化物,则A与水反应的化学方程式为 。
①当X是碱性盐溶液,C分子中有22个电子时,则C的结构式为 ,表示X呈碱性的离子方程式为 。
②当X为金属单质时,X与B的稀溶液反应生成C的离子方程式为
。
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,写出该可逆反应的化学方程式 。t℃时,在密闭恒容的某容器中投入等物质的量的D和水蒸气,一段时间后达到平衡,该温度下反应的平衡常数K=1,D的转化率为 。
(10分)(1)Na ( NaH Na2O2 ) Al3+ + 3AlO2- + 6H2O === 4Al(OH)3↓ (2分)
(2)3NO2 + H2O === 2HNO3 + NO (2分)
①O=C=O
CO32- +H2O  HCO3- +OH-
(2分)
HCO3- +OH-
(2分)
②Fe + 4H+ + NO3- === Fe3+ +NO↑ + 2H2O (2分)
(3)CO + H2O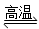 CO2 + H2 50﹪
(2分)
CO2 + H2 50﹪
(2分)
【解析】(1)根据转化关系可知,生成的白色沉淀D可能是氢氧化铝,因此B是应该是是强碱,X是铝盐,所以A可能是钠或过氧化钠或氢化钠等。生成白色沉淀的方程式是 Al3+ + 3AlO2- + 6H2O === 4Al(OH)3↓。
(2)由于E是氧化物,所以A是NO2,E是NO,B是硝酸,则NO2和水反应的方程式是3NO2 + H2O === 2HNO3 + NO。
①当X是碱性盐溶液,C分子中有22个电子时,则C是CO2,结构式是O=C=O。X是碳酸盐,D是碳酸氢盐,碳酸盐溶于水水解显碱性,方程式是CO32- +H2O  HCO3- +OH-。
HCO3- +OH-。
②当X为金属单质时,则X是铁,C是硝酸铁,D是硝酸亚铁。所以X与B的稀溶液反应生成C的离子方程式为Fe + 4H+ + NO3- === Fe3+ +NO↑ + 2H2O 。
(3)根据反应的特点即生成物可知,B是氧气,C是CO2,X是C,D是CO,所以该可逆反应的化学方程式CO + H2O CO2 + H2。设CO和水蒸气的物质的量浓度都是1,转化率是x,则根据化学平衡常数可知
CO2 + H2。设CO和水蒸气的物质的量浓度都是1,转化率是x,则根据化学平衡常数可知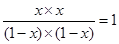 ,解得x=0.5,即转化率是50%。
,解得x=0.5,即转化率是50%。


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | |||||||||||||
| F | G | H | |||||||||||||||
| I | J | K | |||||||||||||||
| L | |||||||||||||||||
| M | N | ||||||||||||||||
| O | |||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | |||||||||||||||||
| j | |||||||||||||||||


 NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是 (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是查看答案和解析>>
科目:高中化学 来源: 题型:
| 周期 主族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com