
【题目】下列过程放出热量的是
A. 液氨气化B. 钠与水反应
C. 碳酸钙分解D. 断开氢气中的H—H键
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置和有关数据如下:

相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 112 | 难溶 |
实验步骤:
在A 中加入4.40g异戊醇、6.00g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯4.55g。
请回答下列问题:
(1)仪器B的名称是_____;B中冷却水是从_____(填“下口”或“上口”)流进的。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的操作是_____________________。
(3)在洗涤、分液操作中,第二次洗涤,用饱和碳酸氢钠溶液洗涤的主要目的是_______,不能用NaOH溶液洗涤的原因是___________。第二次洗涤后,充分振荡,然后静置,待分层后,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)在蒸馏操作中,仪器选择及安装都正确的是下图中的_____(填字母标号),若从130℃ 便开始收集馏分,会使实验的产率______(填“偏高”、“偏低”或“无影响”)。

(5)水的沸点为100℃,比乙酸异戊酯低42℃ ,但仍要先加入MgSO4后过滤再蒸馏,而不是直接蒸馏。结合题中信息分析,下列说法正确的是______(填字母)。
A.水可能会与乙酸异戊酯形成一种“恒沸溶液”(在溶液的某一组成时,在某温度下,混合液同时汽化或同时冷凝),不能进一步提纯,所以要先用MgSO4干燥
B.在加入MgSO4后如不先过滤就蒸馏,加热时硫酸镁的结晶水合物又会脱水
C.如不先用MgSO4吸收水分,蒸馏时水先被蒸出,浪费能源和延长蒸馏时间
D.本实验中要乙酸过量,而不是异戊醇过量,可能的原因是异戊醇比乙酸价格贵;另外异戊醇过量时,异戊醇与乙酸异戊酯沸点相近(小于30℃),蒸馏时完全分离困难
(6)将乙酸异戊酯中的异戊醇除去,是在哪个步骤中除去的______(填字母)。
A.在第一次水洗和后面的分液中除去的
B.在第二次用饱和碳酸氢钠溶液洗涤和后面的分液中除去的
C.在“过滤”中除去的
D.由于本实验中加入过量乙酸,异戊醇已经反应完全,所以不需除杂(异戊醇)了
E.在最后的“蒸馏”步骤中除去的
(7)产物乙酸异戊酯的产率是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.硫酸、纯碱、碳酸氢钠和生石灰分别属于酸、碱、盐和氧化物
B.用丁达尔效应区别FeCl3溶液和Fe(OH)3胶体
C.生石灰与水混合的过程只发生物理变化
D.H2O、CH3COOH、Cu(NH3)4SO4均含有氧,都是氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊为原子序数依次增大的短周期元素。甲、丙处于同一主族,丙、丁、戊处于同一周期,戊原子的最外层电子数是甲、乙、丙原子最外层电子数之和。甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1 mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z的水溶液反应生成盐;丙、戊可组成化合物M。
请回答下列问题:
(1)戊离子的结构示意图为________。
(2)戊的单质与X反应生成的Y和Z的物质的量之比为2∶4,反应中被氧化的物质与被还原的物质的物质的量之比为________。
(3)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式:__________________。
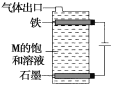
(4)按如图电解M的饱和溶液,写出该电解池中发生反应的总反应方程式:____________________________。将充分电解后所得溶液逐滴加入酚酞溶液中,观察到的现象是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙两个容积均为1L的恒容容器中分别充入2 mol
A. 2 molB和1 molA、l mol B。相同条件下发生如下反应:A(g)+B(g)![]() xC(g) H<0。测得两容器中
xC(g) H<0。测得两容器中![]() 随时间t的变化如图所示。下列说法错误的是 ( )
随时间t的变化如图所示。下列说法错误的是 ( )

A.x可能等于2也可能等于3
B. 若向平衡后的乙容器中充入C,则再次达到平衡时A 的体积分数减小
C. 单独升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同
D. 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25molL-1<c(A)<0.5molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径);Y的单质呈黄色,常见于火山口附近。下列说法正确的是

A. 氧化物的水化物酸性:Y<Z
B. 简单离子半径:W<X<Z
C. W的简单气态氢化物的沸点高于同族其它元素的简单气态氢化物
D. 将标况下等体积的Z单质与Y的低价氧化物同时通入品红溶液中,品红溶液迅速褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2CH3OH(g) ![]() CH3OCH3(g)+H2O(g),某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g),某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度(mol·L-1) | 0.44 | 0.6 | 0.6 |
(1)比较此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”)。
(2)若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)=________;该时间内反应速率v(CH3OH)=________;CH3OH的转化率为________。
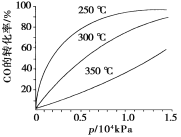
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)===CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH________0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下电离方程式错误的是( )
A.MgCl2=Mg2++2Cl- B.Fe2(SO4)3=2Fe3++3SO42-
C.NaHCO3=Na++H++CO32- D.NaOH=Na++OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图转化关系中,A、B、G、Y都是主族元素组成的单质,其余均是化合物。通常条件下B、E、F、Y均为气体;A、C、H焰色反应均呈黄色;E、F相遇会产生白烟。

请按要求回答下列问题:
(1)化合物F的电子式_______________。
(2)以上反应既属于化合又属于氧化还原反应的有________________(填反应编号)。
(3)E与F反应的化学方程式为________________________________________;
加热条件下C与D的溶液反应的离子反应方程式为_______________________。
(4)G与C的溶液发生反应的离子方程式为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com