
��ѧƽ��״̬I��II��III������������±���
| ��� | ��ѧ����ʽ | ƽ�ⳣ�� | �¶� | |
| 979K | 1173K | |||
| I | Fe(s)+CO2(g) 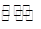 2 FeO(s)+CO(g) 2 FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| II | CO(g)+H2O(g) 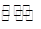 CO2(g)+H2(g) CO2(g)+H2(g) | K2 | 1.62 | b |
| III | Fe(s)+H2O(g)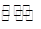 FeO(s)+H2(g) FeO(s)+H2(g) | K3 | a | 1.68 |
C
����������������ݻ�ѧƽ�ⳣ������ʽ����дԭ��֪��K1=[CO]/[CO2]�� K2=[CO2][H2]/[CO][H2O]�� K3=[H2]/[H2O]��������ͬ�¶��£�K3=K1?K2��979Kƽ�ⳣ��a=1.47��1.62=2.38��1173Kƽ�ⳣ��b=1.68/2.15=0.78��A��������������֪a��b����ȷ��B����Ӧ���Ƿ�Ӧǰ���������ʵ�������ķ�Ӧ������ѹǿƽ�ⲻ������ȷ��C��������������֪����Ӧ��ƽ�ⳣ�����¶�����С��ƽ��������У�����D����Ӧ���ƽ�ⳣ�����¶�����С��˵������ӦΪ���ȷ�Ӧ����ȷ��
���㣺���黯ѧƽ�ⳣ���ĸ����������Ի�ѧƽ�ⳣ������ѧƽ���Ӱ�졣


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ������н������·�Ӧ��I2(g)+H2(g)  2HI(g)����֪I2��H2��HI����ʼŨ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.2mol/L����һ�������µ���Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����ǣ� ��
2HI(g)����֪I2��H2��HI����ʼŨ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.2mol/L����һ�������µ���Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����ǣ� ��
| A��HIΪ0.4mol/L | B��H2Ϊ0.15mol/L | C��I2Ϊ0.2mol/L | D��HIΪ0.35mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ڴﵽ��ѧƽ��״̬�Ŀ��淴Ӧ��N2 + 3H2 2NH3 + Q��������������ȷ��
2NH3 + Q��������������ȷ��
| A����Ӧ����������Ũ����� | B����Ӧ����������Ũ�Ȳ��ٱ仯 |
| C�������¶ȣ�ƽ��������NH3��Ũ�ȼ�С | D������ѹǿ�������ڰ��ĺϳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
dz��ɫ��Fe(NO3)2��Һ�д��������µ�ƽ�⣺Fe2++2H2O Fe(OH)2+2H+���ڴ���Һ�м���ϡ���ᣬ����Һ����ɫ�仯Ϊ( )
Fe(OH)2+2H+���ڴ���Һ�м���ϡ���ᣬ����Һ����ɫ�仯Ϊ( )
| A����ɫ���� | B��dz��ɫ��ø�dz | C����� | D�������Ա仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���淴Ӧ2NO2 2NO+O2�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
2NO+O2�����������ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
�ٵ�λʱ��������n molO2��ͬʱ����2n mol NO2
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�ۻ���������ɫ���ٸı��״̬
�ܻ��������ܶȲ��ٸı��״̬
�ݻ�������ƽ����Է����������ٸı��״̬
| A���٢ۢ� | B���ڢۢ� | C���٢ۢ� | D���٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
700��ʱ�����ݻ�Ϊ1 L���ܱ������г���һ������CO2��H2��������Ӧ��
CO2��H2(g)  CO(g)��H2O(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1��:
CO(g)��H2O(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1��:
| ��Ӧʱ��/min | n(CO2)/mol | H2/ mol |
| 0 | 1.50 | 1.00 |
| t1 | | 0.40 |
| t2 | 0.90 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��C��CO2 2CO(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv1��N2��3H2
2CO(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv1��N2��3H2 2NH3(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ
2NH3(����Ӧ����)������Ӧ�ķ�Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ
| A��v1��С��v2���� | B��ͬʱ��С |
| C��v1����v2��С | D��ͬʱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������,�� 4 mol A ����� 2 mol B ������ 2 L ���ܱ������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g��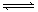 XC��g������ 2 s��Ӧ��ƽ��,��� C ��Ũ��Ϊ 0.6 mol��L��1 ��B�����ʵ���Ϊ1.4 mol,�������м���˵����
XC��g������ 2 s��Ӧ��ƽ��,��� C ��Ũ��Ϊ 0.6 mol��L��1 ��B�����ʵ���Ϊ1.4 mol,�������м���˵����
�������� A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol/(L��s)
�ڷ�Ӧǰ�����ڵ�ѹǿ��ƽ��������ڵ�ѹǿ֮��Ϊ1:1
�� 2 s ʱ����A��ת����Ϊ30�� �� X="2"
������ȷ����
| A���٢ۢ� | B���٢� | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���������ܱ������г���H2��I2��������ӦH2��g��+I2��g�� 2HI��g������H<0,���ﵽƽ���t0ʱ�ı䷴Ӧ��ijһ����,ƽ��ͼ�����£�������˵����ȷ����
2HI��g������H<0,���ﵽƽ���t0ʱ�ı䷴Ӧ��ijһ����,ƽ��ͼ�����£�������˵����ȷ����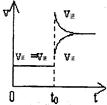
| A��������������ɫ���ƽ����Է����������� | B��ƽ�ⲻ�ƶ�����������ܶ����� |
| C��H2ת��������HIƽ��Ũ�ȱ�С | D��t0ʱ�ı����������ѹ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com