

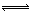 HCO3?+OH? (2分) 制发酵粉或治疗胃酸过多等合理答案 (1分)
HCO3?+OH? (2分) 制发酵粉或治疗胃酸过多等合理答案 (1分)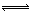 HCO3?+OH?;C为NaHCO3,可制发酵粉或治疗胃酸过多等。
HCO3?+OH?;C为NaHCO3,可制发酵粉或治疗胃酸过多等。

科目:高中化学 来源:不详 题型:单选题
| A.第15列元素的最高价氧化物为R2O5 |
| B.第三周期元素的离子半径,从左到右逐渐减小 |
| C.同周期第ⅡA族与第IIIA族的元素原子序数之差可能为1或11或25 |
| D.只含有非金属元素的化合物不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
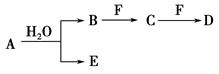
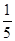 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:_____________________________________;
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:_____________________________________;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:HClO4>H3PO4>H2SO4 | B.氢化物稳定性:H2S>HF>H2O |
| C.碱性:NaOH>Mg(OH)2>Ca(OH)2 | D.氧化性:F2 > Cl2 > Br2 > I2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

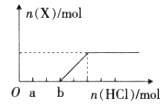
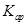 =2.5×
=2.5×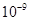 。现将该沉淀放入0.5 mol·
。现将该沉淀放入0.5 mol·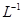 的BaCl2溶液中,其
的BaCl2溶液中,其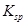 ________(填“增大”、“减小”或“不变”),组成不溶物F的阴离子在溶液中的浓度为________mol·
________(填“增大”、“减小”或“不变”),组成不溶物F的阴离子在溶液中的浓度为________mol·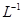 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com