
在室温下的某密闭容中,将某气态烷烃与适量氧气混合,点火使之恰好完全燃烧后,冷却到室温,容器中压强为反应前压强的1/2,该气态烃是
A.甲烷 B.乙烷 C.丙烷 D. 丁烷
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
把0.05 mol NaOH固体分别加入到100 mL下列液体中,溶液的导电能力变化最小的是( )
A.自来水
B.0.5 mol·L-1盐酸
C.0.5 mol·L-1 CH3COOH溶液
D.0.5 mol·L-1 KCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质间的反应肯定无明显实验现象的是 ( )
A.加热经SO2漂白的品红试液
B.将少量SO2通入NaOH溶液中
C.将新制的氯水在阳光下照射
D.将打磨的铝片加入浓NaOH溶液中一段时间
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)白色的Fe(OH)2在空气中发生的颜色变化为
________________________;
(2)写出硅酸钠溶液在空气中变质的化学方程式:
____________________________;
(3)写出用熟石灰吸收氯气制漂白粉的化学方程式:
;
(4)将CaMg3Si4O12改写为氧化物的形式:[gkstk.Com]
__________________________________。[学优高考网gkstk]
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应的反应过程中能量的变化如图所示,图中E1表示正反应的活化能,E2表示逆反应的活化能,下列有关叙述正确的是
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.E1也可表示反应物断键需要吸收的总能量 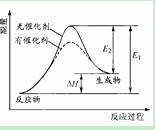
D.△H=E2-E1
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料。下列说法正确的是
A.电极A表面反应之一为NO2-e-+H2O==NO3-+2H+
B.电极B附近的c(NO3-)增大
C.电解质溶液中电流的方向由B到A,电子的流向与之相反
D.该电池工作时,每转移4 mol电子,生成22.4 L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴已知反应Ⅰ:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1266.8kJ/mol
反应Ⅱ:N2(g) + O2(g)== 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式 ,该反应的化学平衡常数的表达式K= (用含K1、K2的代数式表示)。
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为: 。该电池使用过程中,正极附近溶液的pH将 (填“升高”、“降低”或“不变”)。
⑵已知:N2(g) +3H2(g)  2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。
①为提高H2的转化率,宜采取的措施有 (填字母)
A.及时移出氨 B.升高温度 C.使用催化剂 D.循环利用和不断补充N2
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.高锰酸钾溶液:H+、Na+、SO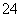 、葡萄糖分子
、葡萄糖分子
B.0.1 mol·L-1 NaOH溶液:K+、Na+、SO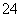 、CO
、CO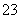
C.0.1 mol·L-1 Na2CO3溶液:K+、Ba2+、NO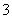 、Cl-
、Cl-
D.0.1 mol·L-1 Na2S溶液:SO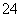 、K+、Cl-、Cu2+
、K+、Cl-、Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH
 CH3COO-+H+。要使[H+]/[CH3COOH]值增大,可采取措施( )
CH3COO-+H+。要使[H+]/[CH3COOH]值增大,可采取措施( )
A.加少量烧碱溶液 B.降低温度
C.加少量冰醋酸 D.加水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com