
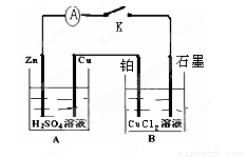
如下图,回答问题:
(1)A装置是将 能转化为 能。
(2)Zn是 极, 电极反应式为 ; Cu电极反应式为 ;
Pt是 极, 电极式为 ; 石墨电极反应式为 。
(3)电解一段时间后发现石墨电极增重6.4g,则外电路中通过的电子的物质的量是 摩尔,
(1)化学能;电能;(2)负;Zn-2e-=Zn2+;2H++2e-=H2↑;阳;2Cl—-2e-=Cl2↑。(3)0.2.(4)
【解析】
试题分析:(1)在两个池中由于A池的电势差大,所以A池是原电池,将化学能转化为电能,B池是电解池,将电能转化为化学能;(2)在原电池中,活动性强的Zn作负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+;活动性弱的电极Cu为正极,电极 Cu电极反应式为2H++2e-=H2↑;在电解池中,由于电极Pt与电源的正极连接,所以是阳极,因为在溶液中阴离子的放电能力Cl->OH-,所以电极式为2Cl—-2e-=Cl2↑。石墨电极为阴极,因为Cu2+的沸点能力大于H+,所以反应式为Cu2++2e-=Cu。(3)电解一段时间后发现石墨电极增重6.4g,则n(Cu)= 6.4g÷64g/mol=0.1mol,因为Cu是+2价的金属,所以每产生1mol的Cu,会转移2mol的电子。现在产生了0.1mol的金属,所以在外电路中通过的电子的物质的量是0.2mol。
考点:考查电化学反应原理、电极反应、电极的判断、反应过程中的电子转移的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:选择题
巴豆酸的结构简式为CH3CH=CHCOOH 现有:①氯化氢,②溴水, ③纯碱溶液,④酸性KMnO4溶液, ⑤乙醇,试根据其结构特点,判断在一定条件下能与巴豆酸反应的物质组合是
A.只有②④⑤ B.只有①③④ C.只有①②③ D.都可以
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
基于实验现象的推论,你认为合理的是( )
选项 | 实验现象 | 推论 |
A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
C | 氨气用于喷泉实验 | 氨气极易溶于水 |
D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
下列各项所述的数字不是6的是 ( )
A.在NaCl晶体中,与一个Na+最近的且距离相等的Cl- 的个数
B.在金刚石晶体中,最小的环上的碳原子个数
C.在二氧化硅晶体中,最小的环上的原子个数
D.在NaCl晶体中,与一个Cl-最近的且距离相等的Na+ 的个数
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
在一定温度下,容器内某一反应中M、N的物质的量浓度随反应时间变化的曲线如图。则下列表述中正确的是( )
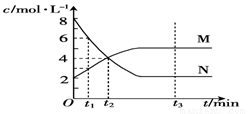
A.该反应的化学方程式为2N ? M
B.t1时,M的浓度是N浓度的2倍
C.t3时,正反应速率大于逆反应速率
D.t2时,正、逆反应速率相等,化学反应达到了平衡
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
电解CuCl2和NaCl的混合溶液,阴极和阳极上最先分别析出的物质是( )
A.H2和Cl2 B.Cu和Cl2 C. H2和O2 D.Cu和O2
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三5月校质检理综化学试卷(解析版) 题型:填空题
[化学—有机化学基础](13分)
对甲基苯甲酸乙酯(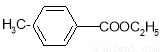 )是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
)是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
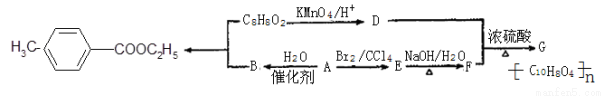 ·
·
(1)D中含有官能团的名称是 ,A-B的反应类型为 。
(2)G的结构简式为 。
(3)写出1种属于酯类且苯环上只有一个取代基的C8H8O2的同分异构体 。
丁香酚( )是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是 (填序号)。
)是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是 (填序号)。
A.NaOH (aq) B.NaHCO3(aq) C.酸性KMnO4(aq) D.FeCl3(aq)
(5)写出合成对甲基苯甲酸乙酯的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3 mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为
A.v (O2)= 0.0l mol·L-1·s-1 B.v (NO)=0.002 mol·L-1·min-1
C.v (H2O)=0.003 mol·L-1·s-1 Dv (NH3)=0.001 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com