
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案科目:高中化学 来源: 题型:解答题
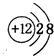
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应是吸热反应 | |
| B. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出热量少 | |
| C. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 | |
| D. | 由热化学方程式 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol可知,1molN2与3molH2放入密闭容器中,在催化剂的作用下反应得到氨气,将释放92kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
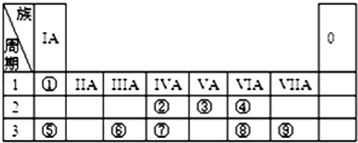
 ,Y中含有的化学键类型是共价键.
,Y中含有的化学键类型是共价键.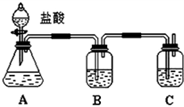
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
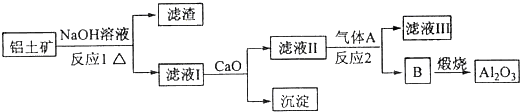
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1471kJ/mol | B. | -1471kJ/mol | C. | 93kJ/mol | D. | -93kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
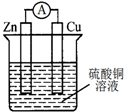
| A. | 电子从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 反应后,锌电极的质量减小 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该高分子是经由缩聚反应得到 | |
| B. | 该高分子的分子式是(C3H3Cl3)n | |
| C. | 聚合物的单体是CHCl=CHClCH3 | |
| D. | 若n为聚合度,则其相对分子质量为97n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com