
【题目】某校学生用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物,请回答下列问题:

(1)冷凝管所起的作用为冷凝回流和导气,冷凝水从___口进入(填“a”或“b”)。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。III中小试管内苯的作用是___。
(3)能说明苯与液溴发生了取代反应的现象是___。
(4)三颈烧瓶中发生反应的化学方程式为___,反应结束后使I中的水流入II中,操作是___。
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤,振荡,分液;②用5%的NaOH溶液洗涤,振荡,分液;③用蒸馏水洗涤,振荡,分液;④加入无水CaCl2粉末干燥;⑤___(填操作名称)。
【答案】a 吸收溴蒸气 III中硝酸银溶液内出现淡黄色沉淀(或测反应后III中硝酸银溶液的pH,其pH变小) ![]() +Br2
+Br2![]()
![]() +HBr 反应结束后关闭K1,打开K2,使水进入Ⅱ中 分馏(或蒸馏)
+HBr 反应结束后关闭K1,打开K2,使水进入Ⅱ中 分馏(或蒸馏)
【解析】
苯和液溴在催化作用下可生成溴苯,同时生成HBr,实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,Ⅲ中小试管内苯可用于除去溴,可用硝酸银溶液检验生成HBr,Ⅳ中氢氧化钠溶液用于吸收尾气,防止污染空气,实验结束,可开启K2,关闭K1和分液漏斗活塞,使I的水倒吸入Ⅱ中可以除去溴化氢气体,以免逸出污染空气,据此分析解答。
(1)冷凝管采用下进上出,即从a进水,使气体与水充分接触,冷凝效果好,故答案为:a;
(2)溴极易挥发,Ⅲ中小试管内苯的作用是除去溴化氢中的溴蒸气,避免干扰溴离子检验,故答案为:吸收溴蒸气;
(3)因从冷凝管出来的气体为溴蒸气和溴化氢,溴易溶于苯,溴化氢不溶于苯,溴化氢能与硝酸银反应生成溴化银沉淀,据此可以说明苯与液溴发生了取代反应,故答案为:Ⅲ中硝酸银溶液内有浅黄色沉淀生成;
(4)装置(Ⅱ)中发生反应的化学方程式为 2Fe+3Br2═2FeBr3、溴化铁对苯和溴单质的反应起到催化剂的作用,![]() +Br2
+Br2 ![]()
![]() +HBr,因装置Ⅱ中含有溴化氢气体能污染空气,使I的水倒吸入Ⅱ中可以除去溴化氢气体,以免逸出污染空气,具体操作方法为:开启K2,关闭K1和分液漏斗活塞,使水进入Ⅱ中,故答案为:
+HBr,因装置Ⅱ中含有溴化氢气体能污染空气,使I的水倒吸入Ⅱ中可以除去溴化氢气体,以免逸出污染空气,具体操作方法为:开启K2,关闭K1和分液漏斗活塞,使水进入Ⅱ中,故答案为:![]() +Br2
+Br2 ![]()
![]() +HBr;开启K2,关闭K1和分液漏斗活塞,使I的水倒吸入Ⅱ中;
+HBr;开启K2,关闭K1和分液漏斗活塞,使I的水倒吸入Ⅱ中;
(5) ①用蒸馏水洗涤,振荡,分液;②用5%的NaOH溶液洗涤,振荡,分液;③用蒸馏水洗涤,振荡,分液;④加入无水CaCl2粉末干燥,得到了含有没有反应的苯和溴苯的混合物,然后通过蒸馏操作,获得纯净的溴苯,故答案为:蒸馏。


科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过__________方法区分晶体、准晶体和非晶体。
(2)基态铜原子的电子排布式为______。
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是_________。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_______个铜原子。
(4)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图:
![]()
该配离子中含有的化学键类型有_______________(填字母序号)。
A.配位键 B.极性键 C.离子键 D.非极性键
(5)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1molFe(CO)5分子中含_____________mol σ键。
(6)某种磁性氮化铁的结构如图所示

N随机排列在Fe构成的正四面体空隙中。正六棱柱底边长为a cm,高为c cm,阿伏加德罗常数的值为NA,则该磁性氮化铁的晶体密度为______g/cm3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___________,![]() 能级上的未成对电子数为________。
能级上的未成对电子数为________。
(2)硫酸镍溶于氨水形成![]() 蓝色溶液。
蓝色溶液。
①![]() 中阴离子的立体构型是_______。
中阴离子的立体构型是_______。
②在![]() 中
中![]() 与
与![]() 之间形成的化学键称为__________,提供孤电子对的成键原子是__________。
之间形成的化学键称为__________,提供孤电子对的成键原子是__________。
③氨的沸点__________(填“高于”或“低于”)膦(![]() ),原因是_____________;氨是__________分子(填“极性”或“非极性”),中心原子的轨道杂化类型为__________。
),原因是_____________;氨是__________分子(填“极性”或“非极性”),中心原子的轨道杂化类型为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物如图的分子式均为C7H8。下列说法正确的是
![]()
A. W、M、N均能与溴水发生加成反应B. W、M、N的一氯代物数目相等
C. W、M、N分子中的碳原子均共面D. W、M、N均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯的产量是衡量一个国家石油化工发展水平的重要标志之一,以乙烯为原料合成的部分产品如图所示。下列有关说法正确的是( )

A.氧化反应有①⑤⑥,加成反应有②③
B.氯乙烯、聚乙烯都能使酸性KMnO4溶液褪色
C.反应⑥的现象为产生砖红色沉淀
D.③的反应条件为浓硫酸、加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取1mL 0.1mol·L-1AgNO3溶液进行如下实验(实验中所用试剂浓度均为0.1mol·L![]() ):
):
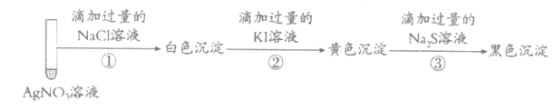
下列说法不正确的是
A.实验①白色沉淀是难溶的AgCl
B.由实验②说明AgI比AgCl更难溶
C.若按①③②顺序实验,看不到黑色沉淀
D.若按②①③顺序实验,看不到白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含锂电解铝废渣(主要含 AlF3、 NaF、LiF、CaO ) 和浓硫酸为原料,制备电池级碳酸锂,同时得副产品冰晶石,其工艺流程如下:
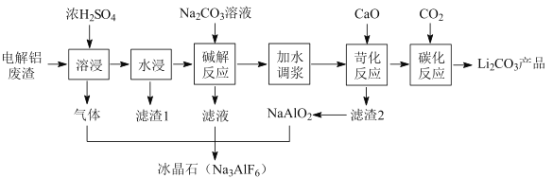
已知LiOH易溶于水,Li2CO3微溶于水。回答下列问题:
(1)电解铝废渣与浓硫酸反应产生的气体化学式为 ___________。滤渣2的主要成分是(写化学式)_________。
(2)碱解反应中, 同时得到气体和沉淀反应的离子方程式为_____________。
(3)一般地说 K>105 时,该反应进行得就基本完全了。苛化反应中存在如下平衡:Li2CO3(s)+Ca2+(aq)2Li+(aq)+ CaCO3(s)通过计算说明该反应是否进行完全________(已知Ksp(Li2CO3) = 8.64×10-4、Ksp(CaCO3) = 2.5×10-9)。
(4)碳化反应后的溶液得到Li2CO3的具体实验操作有:加热浓缩、______、______、干燥。
(5)上述流程得到副产品冰晶石的化学方程式为__________。
(6)Li2CO3是制备金属锂的重要原料, 一种制备金属锂的新方法获得国家发明专利,其装置如图所示:
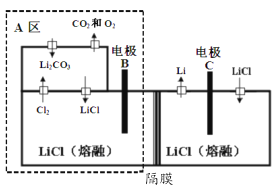
工作时电极 C 应连接电源的______极,阳极的电极反应式为__________ 。该方法设计的 A 区能避免熔融碳酸锂对设备的腐蚀和因________逸出对环境的污染。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四甲基氢氧化铵[(CH3)4NOH]是强碱,常温下甲胺(CH3NH2·H2O)的电离常数为Kb,且pKb=-lgKb=3.38。常温下,在体积均为20mL、浓度均为0.1mol·L-1的四甲基氢氧化铵溶液和甲胺溶液,分别滴加浓度为0.1mol·L-1的盐酸,溶液的导电率与盐酸体积的关系如图所示。
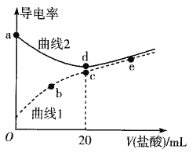
下列说法正确的是
A. 曲线1代表四甲基氢氧化铵溶液
B. 在b、c、e三点中,水的电离程度最大的点是e
C. b点溶液中存在c(H+)=c(OH-)+c(CH3NH2·H2O)
D. 常温下,CH3NH3Cl水解常数的数量级为10-11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。
Ⅰ.经查:①Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10;②Ka(HNO2)=5.1×10-4。请设计最简单的方法鉴别NaNO2和NaCl两种固体______________________
Ⅱ. 某小组同学用如下装置(略去夹持仪器)制备亚硝酸钠
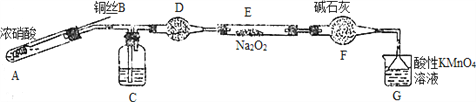
已知:①2NO+Na2O2=2NaNO2; ②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+。
(1)使用铜丝的优点是________________________。
(2)装置A中发生反应的化学方程式为_____________________________。
装置C中盛放的药品是_________;(填字母代号)
A.浓硫酸 B.NaOH溶液 C.水 D.四氯化碳
(3)该小组称取5.000g制取的样品溶于水配成250ml溶液,取25.00ml溶液于锥形瓶中,
用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次实验数据出现异常,造成这种异常的原因可能是_________(填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为___________________。
③该样品中亚硝酸钠的质量分数为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com