
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬×°ÖĆĮ¬½ÓŗĆŗ󣬵ēĮ÷¼ĘÖøÕė·¢ÉśĮĖĘ«×Ŗ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
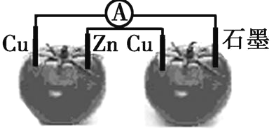
A.Į½øö·¬ĒŃ¼°Ļą¹Ųµē¼«¾ł¹¹³ÉĮĖŌµē³Ų
B.ŠæŹĒøŗ¼«
C.µē×ÓŅĘ¶Æ£ŗŠæ”śĶ£ØÓŅ£©”ś·¬ĒŃ”śŹÆÄ«”śĶ£Ø×ó£©
D.Į½øöĶʬÉĻ¾ł·¢ÉśŃõ»Æ·“Ó¦
”¾“š°ø”æB
”¾½āĪö”æ
×ó²ąĪŖĶ-ŠæĖ®¹ūµē³Ų£¬·¢ÉśµÄŹĒŌµē³Ų·“Ó¦£¬Šæ×÷øŗ¼«”¢·¢ÉśŃõ»Æ·“Ó¦£¬Ķ×÷Õż¼«”¢·¢Éś»¹Ō·“Ó¦£»ÓŅ²ą×°ÖĆŹĒµē½ā³Ų£¬Ķ×÷µē½ā³ŲµÄŅõ¼«”¢·¢Éś»¹Ō·“Ó¦£¬ŹÆÄ«×÷µē½ā³ŲµÄŃō¼«”¢·¢ÉśŃõ»Æ·“Ó¦£¬¾Ż“Ė·ÖĪö½ā“š”£
A”¢×ó²ą·¬ĒŃ¼°Ļą¹Ųµē¼«¹¹³ÉĮĖŌµē³Ų£¬ÓŅ²ą·¬ĒŃ¼°Ļą¹Ųµē¼«¹¹³ÉĮĖµē½ā³Ų£¬¹ŹA“ķĪó£»
B”¢Ķ-Šæ-·¬ĒŃŌµē³ŲÖŠ£¬Zn½Ļ»īĘĆ£¬×÷øŗ¼«£¬¹ŹBÕżČ·£»
C”¢×ó²ą×°ÖĆĪŖŌµē³Ų£¬Šæ×÷øŗ¼«”¢Ķ×÷Õż¼«£»ÓŅ²ą×°ÖĆĪŖµē½ā³Ų£¬Ķ×÷Ņõ¼«”¢ŹÆÄ«×÷Ńō¼«£¬µē×ÓŅĘ¶Æ£ŗŠæ”śĶ(ÓŅ)£¬ŹÆÄ«”śĶ(×ó)£¬µē×Ó²»ÄÜŌŚ·¬ĒŃÖŠŅĘ¶Æ£¬¹ŹC“ķĪó£»
D”¢×ó²ą×°ÖĆĪŖŌµē³Ų£¬Ōµē³ŲÖŠĶĪŖÕż¼«£¬µē¼«ÉĻĒāĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬ÓŅ²ą×°ÖĆŹĒµē½ā³Ų£¬ĶĪŖŅõ¼«£¬Ņõ¼«ÉĻŃōĄė×ӵƵē×Ó·¢Éś»¹Ō·“Ó¦£¬¹ŹD“ķĪó£»
¹ŹŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijÖÖæóŹÆÖŠĢśŌŖĖŲŅŌŃõ»ÆĪļFemOnŠĪŹ½“ęŌŚ£¬ĻÖ½ųŠŠČēĻĀŹµŃé£ŗ½«ÉŁĮæĢśæóŹÆѳʷ·ŪĖ飬³ĘČ”25.0 gѳʷӌÉÕ±ÖŠ£¬¼ÓČėĻ”ĮņĖį³ä·ÖČܽā£¬²¢²»¶Ļ¼ÓČČ”¢½Į°č£¬ĀĖČ„²»ČÜĪļ”£ĻņĖłµĆĀĖŅŗÖŠ¼ÓČė10.0 gĶ·Ū³ä·Ö·“Ó¦ŗó¹żĀĖ”¢Ļ“µÓ”¢øÉŌļµĆŹ£Óą¹ĢĢå3.6 g”£Ź£ĻĀĀĖŅŗÓĆÅضČĪŖ2 mol”¤L£1µÄĖįŠŌKMnO4µĪ¶Ø£¬ÖĮÖÕµćŹ±ĻūŗÄKMnO4ČÜŅŗĢå»żĪŖ25.0 mL”£(ĢįŹ¾£ŗ2Fe3£«£«Cu=2Fe2£«£«Cu2£«£¬8H£«£«MnO4-£«5Fe2£«=Mn2£«£«5Fe3£«£«4H2O”£)
£Ø1£©¼ĘĖćøĆĢśæóŹÆÖŠĢśŌŖĖŲµÄÖŹĮæ·ÖŹż”£_____
£Ø2£©¼ĘĖćŃõ»ÆĪļFemOnµÄ»ÆѧŹ½(m”¢nĪŖÕżÕūŹż)”£_______
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ ³£ĪĀĻĀ£¬Ļņ20 mL 0.01mol/L CH3COOHČÜŅŗÖŠÖšµĪ¼ÓČė0.01mol/L µÄNaOHČÜŅŗ£¬ČÜŅŗÖŠĖ®ĖłµēĄė³öµÄc(H+)Ėę¼ÓČėNaOHČÜŅŗµÄĢå»ż±ä»ÆŹ¾ŅāĶ¼ČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
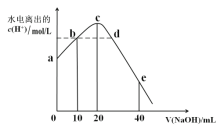
A£®“Óaµ½c£¬“×ĖįµÄµēĄėŹ¼ÖÕŹÜµ½“Ł½ų
B£®a”¢d¶ŌÓ¦µÄׯ×ų±źŹżÖµ·Ö±šŹĒ£ŗ£¾10-12”¢£¾10-7
C£®bµć£ŗ2c(Na+)£½c(CH3COO-)£«c(CH3COOH)
D£®“Ób”ścµÄ¹ż³ĢÖŠ£¬¼Č“ęŌŚ×ÅpH=7µÄµć£¬Ņ²“ęŌŚ×ÅČÜŅŗÖŠĖ®ĖłµēĄė³öµÄc(H+)=10-7µÄµć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)Š“³öĻĀĮŠĪļÖŹµÄµē×ÓŹ½£ŗ
NH4Cl_______________ NaOH__________________
H2O2_________________ HClO_________________
(2)ŅŃÖŖÓŠĻĀĮŠĪļÖŹ£ŗ¢ŁHNO3 ¢ŚĮņµ„ÖŹ ¢ŪNaOH ¢ÜŅŗŗ¤ ¢ŻNa2O2 ¢ŽH2O2 ¢ßCCl4 ¢ąNH4Cl ¢įKBr ¢āO2£¬·Ö±š½«ÕżČ·µÄŠņŗÅĢīČėĻąÓ¦µÄĪ»ÖĆ”£
ŅŌÉĻĪļÖŹÖŠÖ»ŗ¬ÓŠĄė×Ó¼üµÄŹĒ______________£»
Ö»ŗ¬ÓŠ¹²¼Ū¼üµÄŹĒ__________________£»
¼Čŗ¬ÓŠĄė×Ó¼üÓÖŗ¬ÓŠ¹²¼Ū¼üµÄŹĒ____________£»
ŗ¬ÓŠ·Ē¼«ŠŌ¹²¼Ū¼üµÄ»ÆŗĻĪļŹĒ________£»
²»ŗ¬»Æѧ¼üµÄŹĒ__________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ( )
A.ŅŅĻ©”¢SO2ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬ĘäĶŹÉ«ŌĄķĻąĶ¬
B.COŗĶH2»ģŗĻĘųĢåŗĶŃõĘųÖŠ³ä·ÖČ¼ÉÕ£¬Ö»ŅŖ»ģŗĻĘųĢå×ÜĪļÖŹµÄĮæŅ»¶Ø£¬ĻūŗÄŃõĘųµÄĮæŅ»¶Ø
C.ŅŅČ©ŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėĒāĘų·“Ӧɜ³ÉŅŅ“¼£¬·¢ÉśĮĖ»¹Ō·“Ó¦
D.CH2=CH2+HCl![]() CH3CH2CløĆÓŠ»ś·“Ó¦Ó¦ĪŖČ”“ś·“Ó¦
CH3CH2CløĆÓŠ»ś·“Ó¦Ó¦ĪŖČ”“ś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚa L Al2(SO4)3ŗĶ(NH4)2SO4µÄ»ģŗĻČÜŅŗÖŠ¼ÓČėb mol BaCl2£¬Ē”ŗĆŹ¹ČÜŅŗÖŠµÄSO42-ĶźČ«³Įµķ£»Čē¼ÓČė×ćĮæĒæ¼ī²¢¼ÓČČæɵƵ½c mol NH3£¬ŌņŌČÜŅŗÖŠAl3£«µÄÅضČ(mol/L)ĪŖ
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĪüø½ĮĖĒāĘųµÄÄÉĆ×Ģ¼¹ÜµČ²ÄĮĻÖĘ×÷µÄ¶ž“Īµē³ŲŌĄķČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
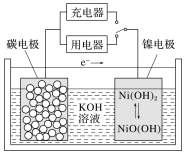
A.³äµēŹ±£¬Ņõ¼«µÄµē¼«·“Ó¦ĪŖ£ŗNi(OH)2£«OH££e£=NiO(OH)£«H2O
B.·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦ĪŖ£ŗH2£2e£=2H+
C.·ÅµēŹ±£¬OH£ŅĘĻņÄųµē¼«
D.³äµēŹ±£¬½«µē³ŲµÄĢ¼µē¼«ÓėĶāµēŌ“µÄøŗ¼«ĻąĮ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÕżČ·µÄŹĒ( )
A.¶”“¼µÄĶ¬·ÖŅģ¹¹Ģå![]() ²»ŗ¬Į¢ĢåŅģ¹¹
²»ŗ¬Į¢ĢåŅģ¹¹![]() ÓŠ7ÖÖ
ÓŠ7ÖÖ
B.ĆŽ”¢Ė攢ĖÜĮĻ¼°ŗĻ³ÉĻš½ŗĶźČ«Č¼ÉÕ¶¼Ö»Éś³ÉCO2ŗĶH2O
C.C6H5Li+CO2”śC6H5COOLi¼Č²»ŹōÓŚ¼Ó³É·“Ó¦Ņ²²»ŹōÓŚČ”“ś·“Ó¦
D.ŅŅĻ©ÄÜŹ¹äåĖ®ĶŹÉ«”¢ŅŅ“¼ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬·¢ÉśµÄ·“Ó¦ĄąŠĶĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
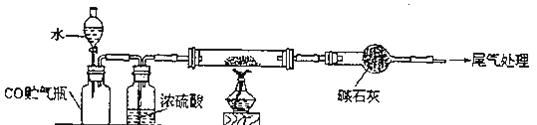
”¾ĢāÄæ”æÄ³ŃŠ¾æŠŌѧĻ°Š”×éÓĆČēĶ¼×°ÖĆ![]() Ģś¼ÜĢصČŅĒĘ÷ĀŌ
Ģś¼ÜĢصČŅĒĘ÷ĀŌ![]() Ģ½¾æŃõ»ÆĢśÓėŅŅ“¼µÄ·“Ó¦£¬²¢¼ģŃé·“Ó¦²śĪļ”£
Ģ½¾æŃõ»ÆĢśÓėŅŅ“¼µÄ·“Ó¦£¬²¢¼ģŃé·“Ó¦²śĪļ”£
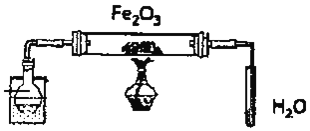
ŅŃÖŖ£ŗ![]() ŅŅ“¼µÄŃõ»Æ²śĪļŹĒŅŅČ©£»
ŅŅ“¼µÄŃõ»Æ²śĪļŹĒŅŅČ©£»
![]() ŅŅ“¼ŗĶŅŅČ©¶¼Ņ×ČÜÓŚĖ®£¬ŅŅ“¼·ŠµćŹĒ75”ę £¬ŹĒ20.8”ę
ŅŅ“¼ŗĶŅŅČ©¶¼Ņ×ČÜÓŚĖ®£¬ŅŅ“¼·ŠµćŹĒ75”ę £¬ŹĒ20.8”ę
£Ø1£©×é×°ŗĆŅĒĘ÷ŗóŠė½ųŠŠµÄ²Ł×÷ŹĒ______£¬Ęä·½·ØŹĒ______
£Ø2£©Ō²µ×ÉÕĘæÖŠŹŌ¼ĮµÄ½į¹¹¼ņŹ½ŹĒ______”£
£Ø3£©±¾ŹµŃé×°ÖĆÓŠŅ»“¦²»ŗĻĄķ£¬Čē²»¼ÓŅŌøĽųæÉÄÜ»į·¢Éś______”£
£Ø4£©¾ÉĻŹöŹµŃ飬¹Ū²ģÖĮŗģÉ«µÄFe2O3Č«²æ±äĪŖŗŚÉ«¹ĢĢ唣Ķ£Ö¹¼ÓČČ£¬ĄäČ“ŗóČ”³öÓ²ÖŹ²£Į§¹ÜÖŠµÄŗŚÉ«¹ĢĢåÉŁŠķŠķÓŚŹŌ¹ÜÖŠ£¬ŌŁ¼ÓČė×ćĮæĻ”ĮņĖį£¬Õńµ“£¬¹ĢĢåČ«²æČܽā£¬µĆµ½³ĪĒåČÜŅŗ£¬ŹµŃé¹ż³ĢÖŠĪ“¹Ū²ģµ½ĘųÅŻ²śÉś”£³ĪĒåČÜŅŗÖŠŅ»¶Øŗ¬ÓŠµÄ½šŹōŃōĄė×ÓŹĒ______¼ģŃéøĆĄė×ӵďµŃéŹĒ______
£Ø5£©ŗŚÉ«¹ĢĢå³É·ÖÓĆFeOxŹ¾”£ÓĆĻĀĮŠ×°ÖĆ²āĮæXÖµ”£
![]() ³ä·Ö·“Ó¦ŗó£¬Ķ£Ö¹ŹµŃéµÄ²Ł×÷ŹĒ_______
³ä·Ö·“Ó¦ŗó£¬Ķ£Ö¹ŹµŃéµÄ²Ł×÷ŹĒ_______
![]() ŹµŃéÖŠ²āµĆŹż¾ŻČēĻĀ
ŹµŃéÖŠ²āµĆŹż¾ŻČēĻĀ![]() ½ųŠŠµÄ·“Ó¦¼ŗĶźČ«
½ųŠŠµÄ·“Ó¦¼ŗĶźČ«![]() £ŗ
£ŗ
æÕÓ²ÖŹ²£Į§¹ÜµÄÖŹĮæ56.0g
Ó²ÖŹ²£Į§¹ÜŗĶFeOxµÄ×ÜÖŹĮæ79.2g
Ó²ÖŹ²£Į§¹ÜŗĶFe·ŪµÄ×ÜÖŹĮæ72.8g£ØĄäČ“µ½ŹŅĪĀ³ĘĮæ![]()
·“Ó¦Ē°øÉŌļ¹Ü¼°ÄŚŹ¢ĪļµÄ×ÜÖŹĮæ48.0g
·“Ó¦ŗóøÉŌļ¹Ü¼°ÄŚŹ¢ĪļµÄ×ÜÖŹĮæ65.6g
¾ŻÉĻŹöŹż¾Ż¼ĘĖć³öX=______
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com