
【题目】水的电离平衡曲线如右图所示,下列说法中,正确的是
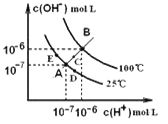
A. 图中A、B、D三点处KW间的关系: B>A>D
B. 100℃,向pH=2的稀硫酸中逐滴加入等体积pH=10的稀氨水,溶液中 c(NH4+)/c(NH3·H2O)减小,充分反应后,溶液到达B点
C. 温度不变,在水中加入适量NH4Cl固体,可从A点变化到C点
D. 加热浓缩A点所示溶液,可从A点变化到B点
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛,可由N2、H2合成NH3。
(1)天然气蒸汽转化法是前获取原料气中H2的主流方法。CH4经过两步反应完全转化为H2和CO2,其能量变化示意图如下:

结合图像,写出CH4通过蒸汽转化为CO2和H2的热化学方程式______________________。
(2)利用透氧膜,一步即获得N2、H2,工作原理如图所示(空气中N2与O2的物质的量之比按4∶1计)
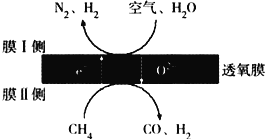
①起还原作用的物质是_________________________。
②膜I侧所得气体![]() =2,CH4、H2O、O2反应的化学方程式是______________________。
=2,CH4、H2O、O2反应的化学方程式是______________________。
(3)甲小组模拟工业合成氨在一恒温恒容的密闭容器中发生如下反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH< 0。t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示,下列说法正确的是____________
2NH3(g) ΔH< 0。t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示,下列说法正确的是____________

A.Ⅰ、Ⅱ两过程到达平衡时,平衡常数:KⅠ<KⅡ
B.Ⅰ、Ⅱ两过程到达平衡时,NH3的体积分数:Ⅰ<Ⅱ
C.Ⅰ、Ⅱ两过程到达平衡的标志:混合气体密度不再发生变化
D.t2时刻改变的条件可以是向密闭容器中加N2和H2混合气
(4)乙小组模拟不同条件下的合成氨反应,向容器充入9.0molN2和23.0molH2,图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。
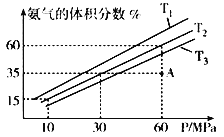
①T1、T2、T3由大到小的排序为______________________________。
②在T2、60MPa条件下,比较A点v正___v逆(填“>”、“<”或“=”),理由是____________。
③计算T2、60Mpa平衡体系的平衡常数Kp=__________。(用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)
查看答案和解析>>
科目:高中化学 来源: 题型:
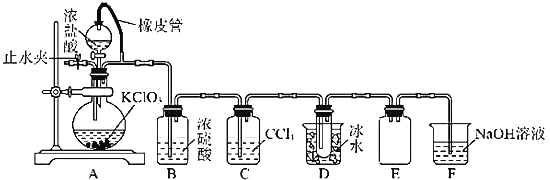
【题目】用浓盐酸与氯酸钾固体反应制氯气时,发现所得气体颜色偏深,经分析该气体主要含有![]() 和
和![]() 两种气体,某研究性学习小组拟用如图所示装置分离制得的混合气体,并测定两种气体的物质的量之比。
两种气体,某研究性学习小组拟用如图所示装置分离制得的混合气体,并测定两种气体的物质的量之比。
Ⅰ.查阅资料:常温下二氧化氯为黄绿色气体,其熔点为![]() ℃,沸点为
℃,沸点为![]() ℃,能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性,能与
℃,能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性,能与![]() 溶液反应生成等物质的量的两种盐,其中一种为
溶液反应生成等物质的量的两种盐,其中一种为![]() 。
。
Ⅱ.制备与分离:
(1)实验加药品前应进行的实验操作是__________。
(2)装置C、E的作用分别是___________、____________。
(3)F中![]() 与
与![]() 溶液反应的离子方程式为___________。
溶液反应的离子方程式为___________。
Ⅲ.测量与计算:反应结束后,测得B、C装置分别增重![]() 和
和![]() ,将D中的液体溶于水,配成
,将D中的液体溶于水,配成![]() 溶液,取
溶液,取![]() 该溶液,调节试样的
该溶液,调节试样的![]() ,加入足量的
,加入足量的![]() 晶体,振荡后,静置片刻;加入指示剂X,用
晶体,振荡后,静置片刻;加入指示剂X,用![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() 。(已知:
。(已知:![]() ,
,![]() )
)
(4)指示剂X为___________溶液,滴定至终点时的现象是溶液由___________色变为_______色。
(5)D装置收集到的![]() 的物质的量为____________。
的物质的量为____________。
Ⅳ.结论:
(6)浓盐酸与氯酸钾固体反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素。其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3以防止腐蚀。
(1)基态碳原子的电子排布图为___。
(2)铬和镍元素都易形成配位化合物:
①[Cr(H2O)4Cl2]Cl2H2O中Cr3+的配位数为___。
②硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是___,在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为____。
③氨是___分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___,氨的沸点高于PH3,原因是___。
(3)镍元素基态原子的价电子排布式为___,3d能级上的未成对电子数为___。
(4)单质铜及镍都是由金属键形成的晶体,元素铜与镍的第二电离能分别为:ICu=1958kJ/mol、INi=1753kJ/mol,ICu>INi的原因是___。
(5)某镍白铜合金的立方晶胞结构如图所示。若合金的密度为dg/cm3,晶胞参数a=___nm。
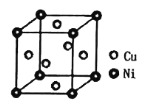
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对图中两极进行必要的连接并填空:
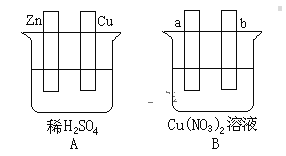
(1)在A图中,使铜片上冒H2气泡。请加以必要连接,则连接后的装置叫____。电极反应式:锌板:____;铜板:_____。
(2)在B图中,使a极析出铜,b极析出氧气。加以必要的连接后,该装置叫____。电极反应式,a极:____;b极:_____。经过一段时间后,停止反应,溶液的pH值____(升高、降低、不变),加入一定量的____后,溶液能恢复至与电解前完全一致。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
(实验Ⅰ)制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。
制备装置如图所示(夹持装置略去):
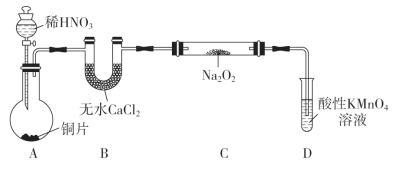
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为____________。
(2)如果没有B装置,C中发生的副反应有_____________、____________。
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。于是进行了适当的改进,改进后提高了NaNO2的纯度,则其改进措施是________________________________。
(实验Ⅱ)测定制取的样品中NaNO2的含量
步骤:
a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:
试管编号 | ① | ② | ③ | ④ | ⑤ |
NaNO2含量/(mg·L-1) | 0 | 20 | 40 | 60 | 80 |
b.称量0.10 g制得的样品,溶于水配成500 mL溶液。取5 mL待测液,加入1 mL M溶液,再加蒸馏水至10 mL并振荡,与标准色阶比较。
(4)步骤b中比较结果是:待测液颜色与③标准色阶相同,则甲同学制得的样品中NaNO2的质量分数是________。
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。
实验方案 | 实验现象 | 实验结论 |
取5 mL待测液,加入______________,振荡,再加入1 mL M溶液,_______________,再振荡,与③标准色阶对比 | _______________ | 维生素C可以有效降低NaNO2的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示:
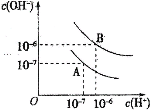
(1)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为______________。
(2)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是________________。
(3)95℃时,向Ba(OH)2溶液中逐滴加入pH=a的盐酸,测得混合溶液的部分pH如表所示。
实验序号 | Ba(OH)2溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
① | 22.00 | 0.00 | 8 |
② | 22.00 | 18.00 | 7 |
③ | 22.00 | 22.00 | 6 |
假设溶液混合前后的体积不变,则a=_________,实验②所得溶液中由水电离产生的c(OH-)=______。
(4)95℃时,将0.1 mol·L-1的NaHSO4溶液与0.1 mol·L-1的Ba(OH)2溶液按下表中甲、乙、丙、丁不同方式混合:
甲 | 乙 | 丙 | 丁 | |
0.1 mol·/span>L-1 Ba(OH)2溶液体积/mL | 10 | 10 | 10 | 10 |
0.l mol·L-1 NaHSO4溶液体积/mL | 5 | 10 | 15 | 20 |
①按丁方式混合后,所得溶液显_____(填“酸”、“碱”或“中”)性。
②写出按乙方式混合后反应的化学方程式_______________________。所得溶液显______(填“酸”、“碱”或“中”)性。
③按甲方式混合,所得溶液的pH为________(混合时,忽略溶液体积的变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.8×10-10,若向50mL 0.018 mol·L-1的AgNO3溶液中加入50mL 0.020mol·L-1的盐酸(不考虑混合后溶液体积的变化)。
计算:
(1)混合溶液的pH。
(2)混合后溶液中的Ag+浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CoCO3为原料采用微波水热法和常规水热法均可制得H2O2分解的高效催化剂CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)。如图是用两种不同方法制得的CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。下列说法不正确的是( )
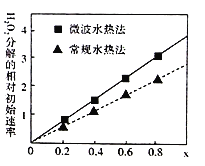
A.由图中信息,可知常规水热法制取的催化剂活性更高,Co2+的催化效果更好
B.微波协同CuO有利于H2O2除去氨态氮。该条件下,1molH2O2将NH3氧化为N2转移电子为2mol
C.常温下0.1moL/L氨水溶液的pH=a,将溶液稀释到原体积的10倍,不能使溶液pH=(a-1)
D.已知煅烧CoCO3时,温度不同,产物不同。在400℃充分煅烧CoCO3,得到固体氧化物的质量2.41g,CO2的体积为0.672L(标况下),则此时所得固体氧化物的化学式为Co3O4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com