分析:(1)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;依据n=cV,m=nM计算需要的Na
2CO
3?8H
2O晶体的质量;
(2)容量瓶作为精密仪器,是用来配置一定物质的量浓度的溶液的主要仪器,不可用于储存和溶解、稀释物质,也不能测量除其规格以外容积的液体体积;
(3)依据配置一定物质的量浓度溶液的一般步骤解答;
(4)根据公式c=
,可以根据影响n和V的因素来分析回答;
(5)依据碳酸钠与盐酸反应的方程式:Na
2CO
3+2HCl═2NaCl+H
2O+CO
2↑计算解答.
解答:
解:(1)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,
还缺少的玻璃仪器是:500ml容量瓶、胶头滴管;
配制0.2mol?L
-1的Na
2CO
3溶液490mL,应选用500ml容量瓶,需要碳酸钠的物质的量:0.2mol?L
-1×0.5L=0.1mol,需要Na
2CO
3?8H
2O的质量为:0.1mol×250g/mol=25.0g;
故答案为:500ml容量瓶、胶头滴管;25.0g;
(2)容量瓶作为精密仪器,是用来配置一定物质的量浓度的溶液的主要仪器,不可用于储存和溶解、稀释物质,也不能测量除其规格以外容积的液体体积,所以
容量瓶不具备的功能有:ABDE;
故答案为:ABDE;
(3)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作;
故答案为:⑤②③①④;
(4)A.称取10.6g 无水Na
2CO
3进行配制,碳酸钠的物质的量为0.1mol,溶液的浓度不变;
B.称量时用了生锈的砝码,称取的溶质的质量偏大,溶质的物质的量偏大,溶液的浓度偏大;
C.往容量瓶转移溶液时,有少量液体溅出,溶质的物质的量偏小,溶液的浓度偏小;
D.Na
2CO
3中含有不溶性杂质,导致溶质的物质的量偏小,溶液的浓度偏小;
E.未洗涤溶解Na
2CO
3的烧杯,导致溶质的物质的量偏小,溶液的浓度偏小;
F.定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏大;
G.容量瓶未干燥即用来配制溶液,对溶质的物质的量和溶液的体积都不会产生影响,溶液浓度不变;
H.砝码与药品位置放反了且用了游码,称取的溶质的质量偏小,溶质的物质的量偏小,溶液的浓度偏小;
下列操作使所配溶液浓度偏大的是:BF;无影响的是:AG;
故答案为:BF;AG;
(5)50ml碳酸钠溶液含碳酸钠的物质的量n=0.05L×0.2mol?L
-1=0.1mol,依据方程式:
Na
2CO
3+2HCl═2NaCl+H
2O+CO
2↑
1 2
0.01mol n(HCl)
所以n(HCl)=0.02mol,
C(HCl)=
=
=0.1 mol/L;
故答案为:0.1 mol/L.



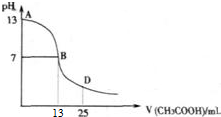
 按图装置进行实验,并回答下列问题:
按图装置进行实验,并回答下列问题: