
【题目】下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述正确的是( )
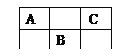
A. B为第二周期的元素
B. C为VA族元素
C. 三种元素都为金属元素
D. C所形成的气态氢化物是三种元素中最稳定的
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.油脂都不能使溴的四氯化碳溶液褪色
D.液化石油气和天然气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙。发生反应:
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s) ![]() CaWO4(s)+2OHˉ(aq) K1
CaWO4(s)+2OHˉ(aq) K1
已知:反应Ⅰ的平衡常数K1理论值如下表,请回答下列问题:
温度/℃ | 25 | 50 | 90 | 100 |
K1 | 79.96 | 208.06 | 222.88 | 258.05 |
(1)判断反应Ⅰ的△S ______0、△H______0(填“>”、“=”或“<”),在______(填“较高”或“较低”)温度下有利于该反应自发进行。
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小。它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s)![]() Ca2+(aq) + WO42ˉ(aq) K2
Ca2+(aq) + WO42ˉ(aq) K2
Ⅲ.Ca(OH)2(s)![]() Ca2+(aq) + 2OHˉ(aq) K3
Ca2+(aq) + 2OHˉ(aq) K3
①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=______(用K2、K3表示)。
②根据反应Ⅱ,右图为不同温度下CaWO4的沉淀溶解平衡曲线。则T1 ____T2(填“>”“=”或“<”)。T1时,向0.5 molLˉ1钨酸钠的碱性溶液中,加入适量Ca(OH)2,反应达到平衡后WO42ˉ的转化率为60%,此时溶液中c(Ca2+)=_______molLˉ1。(假设反应前后体积不变)

(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率。反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3。
①在反应混合液中不直接通入CO2,其理由是_____________;
②用平衡移动原理解释添加酸性物质的理由______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,也常用于鱼类、肉类等食品的染色和防腐,易溶于水,微溶于乙醇。某化学兴趣小组对亚硝酸钠与硫酸反应的气体产物成分及NaNO2性质进行如下探究:

已知:①NO+NO2+2OH-=2NO2-+H2O;
②气体液化的温度:NO2:21℃,NO:152℃。
(1)仪器a的名称是_____________________。
(2)若要验证A中反应生成的气体产物成分且又不能污染环境,仪器的连接顺序为(用字母序号从左→右表示):A、C、______、______、__________。
(3)B中NaOH溶液的作用是_____________________________________。
(4)反应前打开弹簧夹,通入一段时间氮气,其目的是_______________________;关闭弹簧夹,打开分液漏斗活寒,滴入70%硫酸后,A中产生红棕色气体。
(5)①确认A反应产生的气体中含有NO的现象是:_________________________。
②A中反应的化学反应方程式为________________________________。
(6)利用所提供的试剂(NaNO2溶液、KMnO4溶液、KI溶液、稀硫酸、淀粉溶液)设计实验,证明酸性条件下NaNO2具有氧化性________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,如图(Ⅰ)所示:△H1=△H2+△H3 , 根据上述原理和图(Ⅱ)所示,判断各对应的反应热关系中不正确的是( ) 
A.A→F△H=﹣△H6
B.A→D△H=△H1+△H2+△H3
C.△H1+△H2+△H3+△H4+△H5+△H6=0
D.△H1+△H6=△H2+△H3+△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X,Y,Z,W四种元素是元素周期表中连续三个不同短周期的元素,且原子序数依次增大.X,W同主族,Y,Z为同周期的相邻元素.W原子的质子数等于Y,Z原子最外层电子数之和.Y的一个氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)X,Y,Z,W四种元素的符号:X , Y , Z , W .
(2)Z,W两种元素组成的化合物的电子式分别为、 .
(3)X,Y,Z组成的离子化合物的化学式为 , 该化合物中含有的化学键为 , 它与W的最高氧化物的水化物的溶液在加热条件下反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质与用途具有对应关系的是
A.氨气易液化,可用作制冷剂
B.溴化银具有感光性,可用于人工降雨
C.氯化铁具有氧化性,可用了自来水的杀菌消毒
D.氢氧化铝能与氢氧化钠反应,可用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 形成离子键的阴阳离子间只存在静电吸引力
B. HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
C. 第三周期非金属元素含氧酸的酸性从左到右依次增强
D. 只要含有离子键的化合物就是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关电解质溶液的叙述错误的是( )
A. 某H2SO4溶液中![]() =1.0×108,由水电离出的c(H+)=1×10-11 mol·L-1
=1.0×108,由水电离出的c(H+)=1×10-11 mol·L-1
B. 将0.02 mol·L-1 HCl溶液与0.02 mol·L-1 Ba(OH)2溶液等体积混合后,溶液pH约为12
C. 将0.1 mol·L-1的NaOH溶液加水稀释后,由水电离产生的c(H+)·c(OH-)保持不变
D. pH=3的H2SO4溶液,稀释105倍后,溶液的pH<7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com