
| A. | S2-的结构示意图: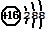 | |
| B. | 过氧化氢的电子式: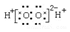 | |
| C. | Ge原子的简化电子排布式:[Ar]4s24p2 | |
| D. | 氯化钠的分子式:NaCl |
分析 A.离子结构示意图书写:圆内数字为原子的质子数,符号表示电性,圆外的弧线为电子层,弧线上的数字为该层上的电子数,离圆最近的弧线表示第一层,依次向外为第二层、第三层等,S2-的质子数为16,核外有18个电子;
B.过氧化氢是共价化合物,无阴阳离子;
C.根据元素原子的核外电子数,结合能量最低原理书写核外电子排布式,根据基态锗原子核外电子排布式书写简化电子排布式;
D.氯化钠为离子化合物,氯化钠中不存在分子.
解答 解:A.硫离子的质子数为16,核外有18个电子,分3个电子层,第一电子层容纳2个电子,第二电子层容纳8个电子,最外层容纳8个电子,结构示意图: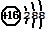 ,故A正确;
,故A正确;
B.过氧化氢为共价化合物,分子中含有2个O-H键和1个O-O键,其电子式为 ,故B错误;
,故B错误;
C.锗为32号元素,根据构造原理,基态锗原子核外电子排布式为:1s22s22p63s23p63d104s24p2或[Ar]3d104s24p2,简化电子排布式[Ar]3d104s24p2,故C错误;
D.NaCl为氯化钠的化学式,氯化钠不存在分子,故D错误;
故选A.
点评 本题考查结结构示意图、电子式、简化电子排布式、分子式等化学用语的判断,为高频考点,题目难度中等,把握化学用语的规范应用是解答的关键,注意理解掌握核外电子排布规律.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源: 题型:选择题
| A. | 从左到右,金属性减弱 | B. | 从左到右,非金属性增强 | ||
| C. | 从左到右,正化合价的数值增大 | D. | 从左到右,原子半径逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
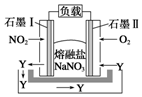 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 环境要求 | 离子或分子 |
| A | Al2(SO4)3溶液中 | K+,AlO${\;}_{2}^{-}$,Cl-,NO${\;}_{3}^{-}$ |
| B | 滴加石蕊试液显蓝色的溶液中 | Na+,K-,SO${\;}_{3}^{2-}$,S2- |
| C | 水电离产生的c(OH-)=10-12mol•L-1的溶液 | ClO-,CO${\;}_{3}^{2-}$,NH${\;}_{4}^{+}$,K- |
| D | 氯气中 | O2,NH3,CO2,HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过干馏可将煤中含有的苯、甲苯等物质分离出来 | |
| B. | 有机玻璃、聚酯纤维(涤纶)均由加聚反应生成 | |
| C. | 地沟油制得的生物柴油和裂化汽油都是烃 | |
| D. | 乙烯与氧气生成环氧乙烷原子利用率为100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
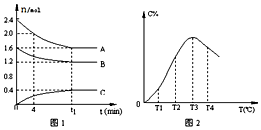
| A. | t1时刻前,混合气体的密度减小,t1时刻后,混合气体的密度不变 | |
| B. | 该反应的平衡常数表达式K=$\frac{c(C)}{{c}^{2}(A)•c(B)}$ | |
| C. | 由T1向T2变化时,V正>V逆 | |
| D. | 此反应的正反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
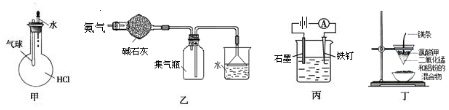
| A. | 如图装置甲:验证HCl气体在水中的溶解度大 | |
| B. | 如图装置乙:可干燥、收集氨气,并吸收多余的氨 | |
| C. | 如图装置丙:防止铁钉生锈 | |
| D. | 如图装置:可制得金属锰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
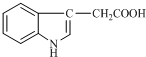 1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )| A. | 吲哚乙酸的分子式是C10H10NO2 | |
| B. | 吲哚乙酸苯环上的二氯代物共有四种(不考虑立体异构) | |
| C. | 吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应 | |
| D. | 1 mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液化石油气主要含乙烯、丙烯和甲烷 | |
| B. | 航空煤油中存在烷烃的同系物 | |
| C. | 相同碳原子数的醇与卤代烃比较,醇在水中溶解度更大 | |
| D. | 聚乙烯和聚甲荃丙烯酸甲酯都是通过加聚反应制得 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com