
| 酸 | 电离常数K |
| HX | 9×10-7 |
| HY | 9×10-6 |
| HZ | 1×10-2 |
| A. | 三种酸的强弱关系:HX>HY>HZ | |
| B. | 反应HZ+Y -=HY+Z -能够发生 | |
| C. | 相同温度下,0.1mol/L的NaX、NaY、NaZ溶液,NaZ溶液pH最大 | |
| D. | 相同温度下,1mol/L HX溶液的电离常数大于0.1mol/L HX |
分析 相同温度下,酸的电离常数越大,则酸的电离程度越大,酸的酸性越强,则酸根离子水解程度越小,结合强酸制取弱酸分析解答.
解答 解:A.相同温度下,酸的电离常数越大,则酸的电离程度越大,酸的酸性越强,则酸根离子水解程度越小,根据电离平衡常数知,这三种酸的强弱顺序是HZ>HY>HX,故A错误;
B.由A知,HZ的酸性大于HY,根据强酸制取弱酸知,HZ+Y-═HY+Z-能发生,故B正确;
C.根据电离平衡常数知,这三种酸的强弱顺序是HZ>HY>HX,酸的电离程度越大,酸根离子水解程度越小,则相同浓度的钠盐溶液,酸根离子水解程度越大的溶液其碱性越强,所以0.1 mol/L的NaX、NaY、NaZ溶液,NaZ溶液pH最小,故C错误;
D.相同温度下,同一物质的电离平衡常数不变,故D错误;
故选B.
点评 本题考查了弱电解质的电离,明确相同温度下电离平衡常数与电解质强弱的关系是解本题关键,易错选项是D,注意温度不变,同一物质的电离平衡常数不变,与溶液的浓度无关,为易错点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa2O2与足量二氧化碳反应转移的电子数为2 NA | |
| B. | 标准状况下22.4L CCl4所含的原子数为5NA | |
| C. | 56g Fe与任何物质完全反应时转移的电子数一定为2NA | |
| D. | 1mol镁与足量氧气或氮气反应均失去2NA的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
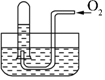 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管.当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )| A. | 可能是N2与NO2的混合气体 | B. | 可能是O2与NO2的混合气体 | ||
| C. | 一定是NO与NO2的混合气体 | D. | 只可能是NO2一种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A组物质 | 熔点/K | B组物质 | 熔点/K |
| NaCl | 1 074 | Na | 317 |
| KCl | 1 049 | Mg | 923 |
| CsCl | 918 | Al | 933 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原混合气体的体积为1.2V | B. | 原混合气体的体积为1.1V | ||
| C. | 反应达平衡时气体B消耗掉0.05V | D. | 反应达到平衡时气体A消耗掉0.05V |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com