
| ���� ���� | ��A | ��A | ��A | ��A | ��A | �� | V��A | 0 |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� |
 ��д������һ����;�������ȣ�
��д������һ����;�������ȣ� ���� ��Ԫ�������ڱ��е�λ�ÿ�֪����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK��
��1��ϡ������ԭ�������Ϊ�ȶ��ṹ����ѧ��������ã�
��2��ͬ�����������ԭ�Ӱ뾶��С��һ����Ӳ�Խ��ԭ�Ӱ뾶Խ��
��3��������������ˮ�����У�������ǿ���Ǹ����ᣬ����Ԫ����K�Ľ�������ǿ�����������صļ�����ǿ��
��4��Ԫ�آݵ�������ΪAl2O3��Ԫ�آܵ�����������Ӧˮ����ΪNaOH�����߷�Ӧ����ƫ��������ˮ��
��5���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ����������õ���֮����û��Ƚ�����֤��
��6����ʾ������γɵĻ�����ΪCO2�ȣ���������������
��� ��Ԫ�������ڱ��е�λ�ÿ�֪����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK��
��1��ϡ������Arԭ�������Ϊ�ȶ��ṹ����ѧ��������ã��ʴ�Ϊ��Ar��
��2��ͬ�����������ԭ�Ӱ뾶��С��һ����Ӳ�Խ��ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶��Cl��N��O���ʴ�Ϊ��Cl��N��O��
��3��������������ˮ�����У�������ǿ����HClO4������Ԫ����K�Ľ�������ǿ�����������صļ�����ǿ���ʴ�Ϊ��HClO4���������أ�
��4��Ԫ�آݵ�������ΪAl2O3��Ԫ�آܵ�����������Ӧˮ����ΪNaOH�����߷�Ӧ����ƫ��������ˮ����Ӧ����ʽΪ��Al2O3+2NaOH=2NaAlO2+H2O���ʴ�Ϊ��Al2O3+2NaOH=2NaAlO2+H2O��
��5���ǽ�����Cl��S���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ������⻯���ȶ��ԣ�HCl��H2S���������õ���֮����û��Ƚ�����֤����Ӧ����ʽΪ��Cl2+H2S=S��+2HCl��
�ʴ�Ϊ��HCl��Cl2+H2S=S��+2HCl��
��6����ʾ������γɵĻ�����ΪCO2�ȣ�������̼����ʽΪ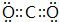 ����������������
����������������
�ʴ�Ϊ��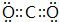 ���������ȣ�
���������ȣ�
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɣ��Ƚϻ�����ע������ԡ��ǽ�����ǿ���Ƚ�ʵ����ʵ��


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
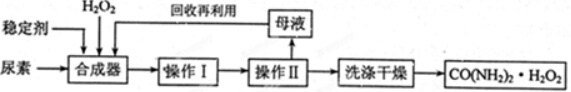
 H2O2+
H2O2+ 6H+=
6H+= Mn2++
Mn2++ O2��+
O2��+ 8H2O��
8H2O��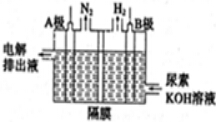
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �Թܱ�� | �� | �� | �� | �� | �� |
| NaNO2����/mg•L-1 | 0 | 20 | 40 | 60 | 80 |
| ʵ�鷽�� | ʵ������ | ʵ����� |
| ȡ5mL ����Һ������һ������ά����C���� �ټ���1mL M��Һ������������ˮ10mL������ ��ܺ�ɫ�Աȣ� | �Ϻ�ɫ�Ȣ�ɫ��dz | ά����C ������Ч����NaNO2�ĺ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£���20mL 0.2mol��L H2A��Һ�еμ�0.2mol/L NaOH��Һ���й��������ʵ����仯��ͼ������1����H2A��II����HA-��III����A2-��������ͼʾ�жϣ�����˵����ȷ�ģ�������
�����£���20mL 0.2mol��L H2A��Һ�еμ�0.2mol/L NaOH��Һ���й��������ʵ����仯��ͼ������1����H2A��II����HA-��III����A2-��������ͼʾ�жϣ�����˵����ȷ�ģ�������| A�� | ��ʹNaHA��Һ�����ԣ����������м������� | |
| B�� | ��NaHA��Һ����ˮ�Ĺ����У�pH��������Ҳ���ܼ�С | |
| C�� | ��V��NaOH��=20mLʱ����Һ������Ũ�ȴ�С��ϵ��c��Na+����c��HA-����c��H+����c��A2-����c��OH-�� | |
| D�� | �������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻ�����Һ��ˮ�ĵ���̶ȱȴ�ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com