
ЁОЬтФПЁП25ЁцЪБЃЌгУ0ЃЎ1molL-1NaOHШмвКЕЮЖЈ20mL 0.1molL-1 H2SO3ШмвКЕФЕЮЖЈЧњЯпШчЭМЫљЪОЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧ

A. aЕуЃКc(H2SO3)+ c(HSO3-)+c(SO32-)=0.1molL-1
B. bЕуЃКc(Na+)>c(HSO3-.)> c(H2SO3)> c(SO32-)
C. ШмвКЕМЕчадb>c
D. aЁЂbЁЂcЁЂdжаЃЌdЕуЫЎЕФЕчРыЖШзюДѓ
ЁОД№АИЁПD
ЁОНтЮіЁП
вђЮЊH2SO3+NaOH=NaHSO3+H2O, NaHSO3+ NaOH= Na2SO3+H2OЃЌaЕуЪБ20mL 0.1molL-1H2SO3ШмвКгы10mL 0.1molL-1NaOH ЛьКЯЗЂЩњЕФЪЧЕквЛИіЗДгІ, ШмвКЮЊH2SO3 КЭNaHSO3ЕФЛьКЯвКЃЛbЕуЪБ20mL 0.1molL-1NaOHЃЌСНепЧЁКУЗДгІЃЌЩњГЩNaHSO3ШмвКЃЛcЕуЪБЮЊNaHSO3КЭNa2SO3ЕФЛьКЯвКЃЌdЕуЪБЮЊNa2SO3ШмвКЁЃ
AИљОнвдЩЯЗжЮіжЊ aЕуЃКШмвКЕФЬхЛ§діДѓЃЌИљОнЮяСЯЪиКуc(H2SO3)+ c(HSO3-)+c(SO32-)<0.1molL-1,ЙЪAДэЮѓЃЛB. bЕуЪБЮЊNaHSO3ШмвКЃЌHSO3-ЕчРыДѓгкЫЎНтЃЌЫљвдРызгХЈЖШДѓаЁЮЊЃКc(Na+)> c(HSO3-.)> c(SO32-)> c(H2SO3)ЃЌЙЪBДэЮѓЃЛC. ШмвКЕМЕчадгыЕчНтжЪШмвКжаРызгХЈЖШКЭРызгЫљДјЕФЕчКЩЪ§гаЙиЁЃcЕуЪБЮЊNaHSO3КЭNa2SO3ЕФЛьКЯвКЃЌЫљвдcЕуРызгХЈЖШДѓгкb,ЕМЕчадЕФb<c,ЙЪCДэЮѓЃЛD. aЕуЮЊH2SO3 КЭNaHSO3ЛьКЯвКЃЛbЕуЮЊNaHSO3ШмвКЃЛcЕуЪБЮЊNaHSO3КЭNa2SO3ЕФЛьКЯвКЃЌdЕуЪБЮЊNa2SO3ШмвКЁЃSO32-ЫЎНтГЬЖШзюДѓЃЌЫЎНтДйНјЫЎЕФЕчРыЃЌЫљвдaЁЂbЁЂcЁЂdжаЃЌdЕуЫЎЕФЕчРыЖШзюДѓЃЌЙЪDе§ШЗЃЛД№АИЃКDЁЃ


 зДдЊЗЛШЋГЬЭЛЦЦЕМСЗВтЯЕСаД№АИ
зДдЊЗЛШЋГЬЭЛЦЦЕМСЗВтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯПЩвдгУЗЯЬњаМжЦБИЛюадFe3O4ЃЌСїГЬШчЯТЭМЃК

(1)дкжЦБИЙ§ГЬжаЃЌвЊНЋПщзДЙЬЬхдСЯЗлЫщЁЂФЅГЩЗлФЉЃЌзїгУЪЧ________________________
(2)дкКЯГЩГиРяЩњГЩFe3O4ЕФРызгЗНГЬЪНЮЊ__________________________
(3)ИљОнСїГЬПЩжЊЃЌХфСЯжааФКмПЩФмЪЙЛьКЯЮяжаЕФFe2O3гыFeЮяжЪЕФСПжЎБШНгНќ________
(4)ФГЭЌбЇРћгУЗЯЬњаМЃЈКЌFeКЭFe2O3ЃЉРДжЦШЁFeCl3ЁЄ6H2OОЇЬхЃЌЭЌЪБВтЖЈЛьКЯЮяжаЬњЕФжЪСПЗжЪ§ЃЌзАжУШчЭМЃЈМаГжзАжУТдЃЌЦјУмадвбМьбщЃЉЃК
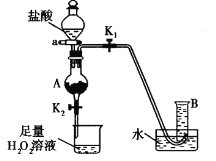
ВйзїВНжшШчЯТЃК
IЃЎДђПЊЕЏЛЩМаK1ЁЂЙиБеЕЏЛЩМаK2ЃЌВЂДђПЊЛюШћaЃЌЛКТ§ЕЮМгбЮЫсЁЃ
ЂђЃЎЕБЁЁЪБЃЌЙиБеЕЏЛЩМаK1ДђПЊЕЏЛЩМаK2ЃЌЕБAжаШмвКЭъШЋНјШыЩеБКѓЙиБеЛюШћaЁЃ
ЂѓЃЎНЋЩеБжаШмвКеєЗЂХЈЫѕЁЂРфШДНсОЇЁЂЙ§ТЫКѓЕУЕНFeC13ЁЄ6H2OОЇЬхЁЃ
ЧыЛиД№ЃК
Ђй ВйзїЂђжаЁАЁЁЁБЕФФкШнЪЧ______________ЃЌЩеБжаЕФЯжЯѓЪЧ_________________ЃЌВЂгаЦјХнВњЩњЁЃЯргІЕФЗНГЬЪНЪЧ________________ЁЂ________________ЁЃЃЈЪЧРызгЗДгІЕФаДРызгЗНГЬЪНЃЉ
ЂкШєЛьКЯЮяжЪСПЮЊm gЃЌЪЕбщНсЪјКѓВтЕУBжаЫљЕУЕФЦјЬхЪЧV mLЃЈБъзМзДПіЪБЃЉЃЌИУЭЌбЇгЩДЫМЦЫуГіДЫЗЯЬњаМжаЬњЕФжЪСПЗжЪ§ЪЧ![]() ЃЌИУЪ§жЕБШЪЕМЪЪ§жЕЦЋЕЭЃЌШєЪЕбщЙ§ГЬВйзїЮоЮѓЃЌЦЋЕЭЕФдвђЪЧ______________________ЁЃ
ЃЌИУЪ§жЕБШЪЕМЪЪ§жЕЦЋЕЭЃЌШєЪЕбщЙ§ГЬВйзїЮоЮѓЃЌЦЋЕЭЕФдвђЪЧ______________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУ50mL 0.50 mol/LбЮЫсгы50 mL 0.55 mol/L NaOHШмвКдкШчЭМЫљЪОЕФзАжУжаНјаажаКЭЗДгІЁЃЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃЛиД№ЯТСаЮЪЬтЃК

ЃЈ1ЃЉЙлВьЪЕбщзАжУЃЌЭМжаЩаШБЩйЕФвЛжжВЃСЇгУЦЗЪЧ__________ЁЃ
ЃЈ2ЃЉЩеБМфЬюТњЫщжНЬѕЕФзїгУЪЧ_________________________ЁЃ
ЃЈ3ЃЉДѓЩеБЩЯПкВЛИЧгВжНАхЃЌВтЕУЕФжаКЭШШЪ§жЕ __________ЃЈЬюЁАЦЋДѓЁЂЦЋаЁЁЂЮогАЯьЁБЃЉЁЃ
ЃЈ4ЃЉЪЕбщжаИФгУ55mL 0.50 mol/LбЮЫсгы55mL 0.55 mol/L NaOHШмвКНјааЗДгІЃЌгыЩЯЪіЪЕбщЯрБШЃЌЫљЗХГіЕФШШСП__________ ЃЈЬюЁАЯрЕШЁЂВЛЯрЕШЁБЃЉЃЌЫљЧѓжаКЭШШ__________ ЃЈЬюЁАЯрЕШЁЂВЛЯрЕШЁБЃЉЁЃ
ЃЈ5ЃЉдкжаКЭШШВтЖЈЪЕбщжаЃЌШєгУЯрЭЌХЈЖШКЭЬхЛ§ЕФАБЫЎДњЬцNaOHШмвКНјааЪЕбщЃЌВтЕУЕФжаКЭШШЕФЪ§жЕЛс____ЃЈЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЁАВЛБфЁБЃЉдвђЪЧ_____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУЯТСаЪЕбщзАжУНјааЯргІЪЕбщ,ФмДяЕНЪЕбщФПЕФЕФЪЧ(ЁЁЁЁ)

A.гУЭМ1ЫљЪОзАжУ(е§ЗХ)ПЩЪеМЏNOЦјЬх
B.гУЭМ2ЫљЪОзАжУПЩЮќЪеЖргрАБЦјЧвФмЗРжЙЕЙЮќ
C.гУЭМ3ЫљЪОзАжУПЩЪЕЯжЗДгІ:Cu+2H2O![]() Cu(OH)2+H2Ёќ
Cu(OH)2+H2Ёќ
D.гУЭМ4ЫљЪОзАжУПЩЗжРыввДМ(ЗаЕу78.4 Ёц)гыЖўМзУб(ЗаЕу24.9 Ёц)ЕФЛьКЯЮя
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЃЌЬхЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌNO2КЭN2O4жЎМфЗЂЩњЗДгІЃК2NO2ЃЈgЃЉЃЈКьзиЩЋЃЉ![]() N2O4gЃЉЃЈЮоЩЋЃЉЃЌШчЭМЫљЪОЃЎ
N2O4gЃЉЃЈЮоЩЋЃЉЃЌШчЭМЫљЪОЃЎ

ЃЈ1ЃЉЧњЯп ЃЈЬюЁАXЁБЛђЁАYЁБЃЉБэЪОNO2ЕФЮяжЪЕФСПЫцЪБМфЕФБфЛЏЧњЯпЃЎ
ЃЈ2ЃЉШєНЕЕЭЮТЖШЃЌдђvЃЈе§ЃЉ ЃЌvЃЈФцЃЉ ЃЎЃЈЬюЁАМгПьЁБЛђЁАМѕТ§ЁБЛђЁАВЛБфЁБЃЉЃЎ
ЃЈ3ЃЉШєЩЯЪіЗДгІдкМзЁЂввСНИіЯрЭЌШнЦїФкЭЌЪБНјааЃЌЗжБ№ВтЕУМзжаvЃЈNO2ЃЉ=0.3mol/ЃЈLsЃЉЃЌввжаvЃЈN2O4ЃЉ=6mol/ЃЈLminЃЉЃЌдђ жаЗДгІИќПьЃЎ
ЃЈ4ЃЉдк0ЕН3minжаФкN2O4ЕФЗДгІЫйТЪЮЊ ЃЎ
ЃЈ5ЃЉЯТСаа№ЪіФмЫЕУїИУЗДгІвбДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧЃЈЬюБъКХЃЉ ЃЛ
AЃЎvЃЈNO2ЃЉ=2vЃЈN2O4ЃЉ |
BЃЎШнЦїФкбЙЧПВЛдйЗЂЩњБфЛЏ |
CЃЎXЕФЬхЛ§ЗжЪ§ВЛдйЗЂЩњБфЛЏ |
DЃЎШнЦїФкЦјЬхдзгзмЪ§ВЛдйЗЂЩњБфЛЏ |
EЃЎЯрЭЌЪБМфФкЯћКФn molЕФYЕФЭЌЪБЩњГЩ2n molЕФX
FЃЎЯрЭЌЪБМфФкЯћКФn molЕФYЕФЭЌЪБЯћКФ2n molЕФXЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСђЕЅжЪМАЦфЛЏКЯЮядкЛЏЙЄЩњВњЁЂЮлЫЎДІРэЕШСьгђгІгУЙуЗКЁЃ
ЃЈ1ЃЉУКжЦЕУЕФЛЏЙЄдСЯЦјжаКЌгаєЪЛљСђ(O=C=S)ЃЌИУЮяжЪПЩзЊЛЏЮЊH2SЃЌжївЊЗДгІШчЯТЃК
i.ЫЎНтЗДгІЃКCOS(g)+H2O(g)![]() H2S(g)+CO2(g) ЁїH1
H2S(g)+CO2(g) ЁїH1
ii.ЧтНтЗДгІЃКCOS(g)+H2(g)![]() H2S(g)+CO(g) ЁїH2
H2S(g)+CO(g) ЁїH2
вбжЊЗДгІжаЯрЙиЕФЛЏбЇМќМќФмЪ§ОнШчЯТБэЃК

ЂйКуЮТКубЙЯТЃЌУмБеШнЦїжаЗЂЩњЗДгІiЁЃЯТСаЪТЪЕФмЫЕУїЗДгІiДяЕНЦНКтзДЬЌЕФЪЧ_______ЁЃ(ЬюБъКХ)
aЃЎШнЦїЕФЬхЛ§ВЛдйИФБф bЃЎЛЏбЇЦНКтГЃЪ§ВЛдйИФБф cЃЎЛьКЯЦјЬхЕФУмЖШВЛдйИФБф dЃЎаЮГЩ1molHЁЊOМќЃЌЭЌЪБаЮГЩ1molHЁЊSМќ

ЂквЛЖЈЬѕМўЯТЃЌУмБеШнЦїжаЗЂЩњЗДгІiЃЌЦфжаCOS(g)ЕФЦНКтзЊЛЏТЪ(ІС)гыЮТЖШ(T)ЕФЙиЯЕШчЭМЫљЪОЁЃдђAЁЂBЁЂCШ§ЕуЖдгІЕФзДЬЌжаЃЌv(COS)=v(H2S)ЕФЪЧ____________ЁЃ(ЬюБъКХ)

ЂлЗДгІiiЕФе§ЁЂФцЗДгІЕФЦНКтГЃЪ§(K)гыЮТЖШ(T)ЕФЙиЯЕШчЭМЫљЪОЃЌЦфжа БэЪОФцЗДгІЕФЦНКтГЃЪ§(KФц)ЕФЪЧ__________(ЬюЁАAЁБЛђЁАBЁБ)ЁЃT1ЁцЪБЃЌЯђШнЛ§ЮЊ10LЕФКуШнУмБеШнЦїжаГфШы2molCOS(g)КЭ1molH2(g)ЃЌЗЂЩњЗДгІiiЃЌCOЕФЦНКтзЊЛЏТЪЮЊ___________ЁЃ
ЃЈ2ЃЉЙ§ЖўСђЫсЪЧвЛжжЧПбѕЛЏадЫсЃЌЦфНсЙЙЪНЮЊ
ЂйAg+ДпЛЏЯТЃЌS2O82-гыMn2+дкЫЎШмвКжаЩњГЩSO42-КЭMnO4-ЃЌИУЗДгІРызгЗНГЬЪН____________ЁЃ
ЂкЙЄвЕЩЯПЩгУЖшадЕчМЋЕчНтСђЫсКЭСђЫсяЇЛьКЯШмвКЕФЗНЗЈжЦБИЙ§ЖўСђЫсяЇЁЃзмЗДгІЕФРызгЗНГЬЪНЮЊ____________________________________ЁЃ
ЃЈ3ЃЉNaHSПЩгУгкЮлЫЎДІРэЕФГСЕэМСЁЃвбжЊЃК25ЁцЪБЃЌЗДгІHg2+(aq)+HS-(aq)HgS(s)+H+(aq)ЕФЦНКтГЃЪ§K=1.75ЁС1038ЃЌH2SЕФЕчРыЦНКтГЃЪ§Ka1=1.0ЁС10-7ЃЌKa2=7.0ЁС10-15ЁЃ
ЂйNaHSЕФЕчзгЪНЮЊ____________________ЁЃ
ЂкKsp(HgS)=_____________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗДгІA(g)+3B(g)![]() 2C(g)+2D(g)ЃЌдкЫФжжВЛЭЌЧщПіЯТгУВЛЭЌЮяжЪБэЪОЕФЗДгІЫйТЪЗжБ№ШчЯТЃЌЦфжаЗДгІЫйТЪзюДѓЕФЪЧЃЈ ЃЉ
2C(g)+2D(g)ЃЌдкЫФжжВЛЭЌЧщПіЯТгУВЛЭЌЮяжЪБэЪОЕФЗДгІЫйТЪЗжБ№ШчЯТЃЌЦфжаЗДгІЫйТЪзюДѓЕФЪЧЃЈ ЃЉ
A. Ід(C)=4 molЁЄ(LЁЄs)-1B. Ід(B)=6 molЁЄ(LЁЄs)-1
C. Ід(A)=3 molЁЄ(LЁЄs)-1D. Ід(D)=2molЁЄ(LЁЄs)-1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГгаЛњЮяНсЙЙМђЪНЮЊЃК ЃЌдђгУNaЁЂNaOHЁЂNaHCO3гыЕШЮяжЪЕФСПЕФИУгаЛњЮяЧЁКУЗДгІЪБЃЌЯћКФNaЁЂNaOHЁЂNaHCO3ЕФЮяжЪЕФСПжЎБШЮЊ ЃЈ ЃЉ
ЃЌдђгУNaЁЂNaOHЁЂNaHCO3гыЕШЮяжЪЕФСПЕФИУгаЛњЮяЧЁКУЗДгІЪБЃЌЯћКФNaЁЂNaOHЁЂNaHCO3ЕФЮяжЪЕФСПжЎБШЮЊ ЃЈ ЃЉ
A. 3ЁУ3ЁУ2 B. 3ЁУ2ЁУ1 C. 1ЁУ1ЁУ1 D. 3ЁУ2ЁУ2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвдЯТУќЬтЃЌЮЅБГЛЏбЇБфЛЏЙцТЩЕФЪЧ ЃЈ ЃЉ
A. ЪЏФЋжЦГЩН№ИеЪЏ B. УКМгЧтБфГЩШЫдьЪЏгЭ
C. ЫЎБфГЩЦћгЭ D. ИЩБљзЊЛЏГЩдзгОЇЬх
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com