
现有Fe、FeO、Fe2O3和Fe3O4组成的混合物,取一定质量,加入100 mL 4 mol/L的盐酸,混合物恰好完全溶解,放出a mL(标准状况下)的气体,所得溶液中加入KSCN溶液无血红色出现。若取等质量的该混合物,用足量的CO还原可得铁单质的质量为
A.2.8g B.5.6g C. 8.4g D.11.2 g
科目:高中化学 来源: 题型:
Ⅰ. ①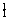 H与
H与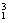 H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷
H;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷
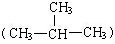 ;④甲烷(CH4)与丙烷(C3H8)。
;④甲烷(CH4)与丙烷(C3H8)。
(1)互为同位素的是______(填序号,下同)。(2)互为同系物的是______。
(3)互为同分异构体的是______。(4)互为同素异形体的是______。
II. A~E等几种烃分子的球棍模型如下图所示,据此回答下列问题。
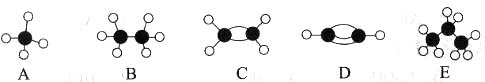
(1)D的化学式为__________________,A的二氯取代物有____________种。
(2)可作为植物生长调节剂的是________________________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
2012年5月15日,CCTV对“南澳一号”沉船的考古进行了两个小时的现场直播,从沉船中发现了大量宋代精美瓷器,体现了灿烂的中华文明。青花瓷胎体的原料——高岭土[Al2Si2O5(OH)x],可掺进瓷石制胎,青花瓷釉料的成分主要是钾长石(KAlSi3O8),在1 300 ℃左右一次烧成的釉可形成精美的青花瓷。
(1)下列说法正确的是________(填序品)。
A.高岭土分子中x=2
B.钾长石能完全溶解在盐酸中形成澄清的溶液
C.烧制青花瓷过程中发生了复杂的物理变化和化学变化
D.青花瓷、玻璃、水泥都属于硅酸盐产品
(2)在“南澳一号”考古直播过程中,需用高纯度SiO2制造的光纤。如图是用海边 的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
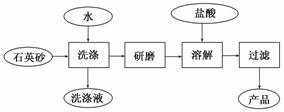
①洗涤石英砂的目的是________________________________________________。
②二氧化硅与氢氧化钠溶液反应的离子方程式是______________________________
________________________________________________________________________。
③在以上流程中,要将洗净的石英砂研磨成粉末,目的是
________________________________________________________________________。
④工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1∶1。下列说法正确的是________(填序号)。
A.SiC是一种传统的无机非金属材料
B.制造粗硅时的反应为:2SiO2+5C Si+SiC+4CO↑
Si+SiC+4CO↑
C.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.纯净的SiO2只能用于制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验的操作、现象和解释或结论都正确的是
|
| 操 作 | 现 象 | 解释或结论 |
| A | 向装有Fe(NO3)2溶液的试 管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| B | 向饱和Na2CO3溶液中通人 足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 |
| C | 向棕黄色的FeCl3溶液 中加入足量的Mg粉 | 溶液变成浅绿色 | 2Fe3++Mg=2Fe2+ + Mg2+ |
| D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+==Cu+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学通过如下实验探究反应原理并验证产物。
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深。
(1)该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH)2•xMgCO3]
(2)为了确定产物,进行以下定性实验:
| 实验序号 | 实 验 | 实验现象 | 结 论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 安静燃烧, 火焰呈淡蓝色 | 气体成分为 ① |
| 实验Ⅲ | 将实验I中的白色不溶物滤出、洗涤,取少量加入足量 ② |
③ | 白色不溶物中含有MgCO3 |
| 实验Ⅳ | 取实验Ⅲ中的滤液,向其中加入适 量 ④ 稀溶液 | 产生白色沉淀,溶液红色变浅 | 溶液中存在CO32- 离子 |
实验Ⅲ中洗涤的操作方法是 。
(3)为进一步确定实验I的白色不溶物的成分,进行以下定量实验,装置如图所示:
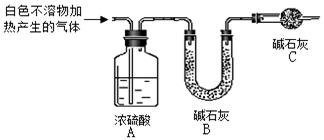
称取干燥、纯净的白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
装置C的作用是 ;
白色不溶物的化学式为 。
(4)写出镁与饱和碳酸氢钠溶液反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关氨气的实验较多,下列对这些实验或实验原理的分析中,正确的是( )
A.某同学将收集到的一大试管氨气倒扣在盛满水的烧杯中,充分吸收后试管中还有少量气体,该同学用红色石蕊试纸检验该气体中可能含有氨气
B.氨水中滴入酚酞变红,是因为氨气能电离出氢氧根离子
C.因氨水中的氨主要以NH3·H2O的形式存在,故25%的氨水是指每100 g氨水中含NH3·H2O 25 g
D.NH3·H2O的热不稳定性可以解释实验室中用加热氨水的方法制取氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com