
【题目】在Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O反应中
CuSO4+SO2↑+2H2O反应中
①元素被氧化,是氧化剂.
②用双线桥标出该反应电子转移的方向和数目 .
Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
③若有2.4mol的H2SO4参与反应,则被还原的H2SO4为g,生成标况下的二氧化硫气体L.
【答案】Cu;硫酸;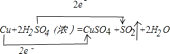 ;117.6;26.88
;117.6;26.88
【解析】解:①Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O中,铜元素的化合价由0价→+2价,失电子被氧化,硫元素的化合价由+6价→+4价,所以硫酸得电子作氧化剂,所以答案是:Cu;硫酸;②铜失电子数=1(2﹣0)=2,硫酸得电子数=1(6﹣4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目为:
CuSO4+SO2↑+2H2O中,铜元素的化合价由0价→+2价,失电子被氧化,硫元素的化合价由+6价→+4价,所以硫酸得电子作氧化剂,所以答案是:Cu;硫酸;②铜失电子数=1(2﹣0)=2,硫酸得电子数=1(6﹣4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目为: 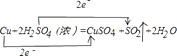 ,所以答案是:
,所以答案是:  ;③该反应中有一半的硫酸是氧化剂,一半的硫酸起酸的作用,所以若有2.4mol的H2SO4参与反应,则被还原的H2SO4的物质的量是1.2mol,其质量=1.2mol×98g/mol=117.6g,由反应可知生成生成标况下的二氧化硫气体为2.4mol×
;③该反应中有一半的硫酸是氧化剂,一半的硫酸起酸的作用,所以若有2.4mol的H2SO4参与反应,则被还原的H2SO4的物质的量是1.2mol,其质量=1.2mol×98g/mol=117.6g,由反应可知生成生成标况下的二氧化硫气体为2.4mol× ![]() ×22.4L/mol=26.88L,
×22.4L/mol=26.88L,
所以答案是:117.6;26.88.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.某些生活垃圾可用于焚烧发电
B.地沟油禁止食用,但可以用来制肥皂或生物柴油
C.石油裂解主要是为了获得气态不饱和短链烃
D.煤是由有机物和无机物组成的复杂的混合物,其中含有焦炭、苯、甲苯等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)![]() 2SO3(g) ΔH=190 kJ·mol1
2SO3(g) ΔH=190 kJ·mol1
(1)该反应所用的催化剂对反应正向移动的影响是________________(填“促进”“抑制”或“无影响”),该反应450℃时的平衡常数________500℃时的平衡常数(填“大于”“小于”或“等于”)。
(2)该热化学反应方程式的意义是________________________________。
(3)下列描述中能说明上述反应已达平衡的是________。
a.v(O2)正=2v(SO3)逆
b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5 L的密闭容器中充入0.20 mol SO2和0.10 mol O2,半分钟后达到平衡,测得容器中含SO3 0.18 mol,则v(O2)=________mol·L1·min1;若继续通入0.20 mol SO2和0.10 mol O2,则平衡________移动(填“向正反应方向”“向逆反应方向”或“不”),再次达到平衡后,________mol<n(SO3)<________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界为人类提供了多种多样的营养物质,下列有关营养物质的说法正确的是( )
A. 食用纤维素、蛋白质、脂肪和植物油都是高分子化合物
B. 棉花和蚕丝的主要成份都是纤维素
C. 麦芽糖、淀粉、纤维素都可以发生水解反应
D. 油脂都不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作错误的是( )
A.用药匙取用粉末状或小颗粒状固体
B.用胶头滴管滴加少量液体
C.给盛有 ![]() 体积液体的试管加热
体积液体的试管加热
D.倾倒液体时试剂瓶标签面向手心
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关CuSO45H2O的叙述正确的是( )
A.1 mol CuSO45H2O的质量为250g/mol
B.125g CuSO45H2O的物质的量为0.5 mol
C.CuSO45H2O的摩尔质量为250g
D.配制100mL 0.1mol/L 硫酸铜溶液需要CuSO45H2O 1.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、稀硫酸、石灰水和氯化铜溶液之间的反应关系如图所示,图中两圆相交部分表示物质间发生了反应.写出A、B、C、D处发生反应的离子方程式. 
A:;
B:;
C:;
D: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com