
| A、邻二甲苯可作生产D的原料 |
| B、E可发生银镜反应 |
| C、E可与FeCl3发生显色反应 |
| D、F与D的相对分子质量相等 |
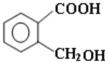 ,E在浓硫酸存在的条件下生成含五元环的化合物F,则F为
,E在浓硫酸存在的条件下生成含五元环的化合物F,则F为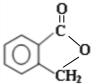 ,据此解答.
,据此解答. ,E在浓硫酸存在的条件下生成含五元环的化合物F,则F为
,E在浓硫酸存在的条件下生成含五元环的化合物F,则F为 ,
,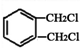 ,在发生水解反应得到
,在发生水解反应得到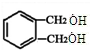 ,进一步氧化可以得到邻苯二甲醛,故A正确;
,进一步氧化可以得到邻苯二甲醛,故A正确; ,没有醛基,不能发生银镜反应,故B错误;
,没有醛基,不能发生银镜反应,故B错误; ,没有酚羟基,不能与FeCl3发生显色反应,硅C错误;
,没有酚羟基,不能与FeCl3发生显色反应,硅C错误; ,与邻苯二甲醛互为同分异构体,二者相对分子质量相等,故D正确,
,与邻苯二甲醛互为同分异构体,二者相对分子质量相等,故D正确,

 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
| A、①④ | B、②⑤ | C、③⑤ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光导纤维的材料是晶体硅 |
| B、金属越活泼,发现和使用的年代越早 |
| C、合理使用化肥有利于提高农作物产量 |
| D、高毒、高效、高残留化合物可用作未来粮食生产的杀虫剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述I | 陈述Ⅱ |
| A | 蛋白质和淀粉都是高分子化合物 | 蛋白质和淀粉水解最终产物均是葡萄糖 |
| B | 汽油和植物油都属于烃 | 汽油和植物油都可以燃烧 |
| C | 盐酸和氨水能溶解Al(OH)3 | Al(OH)3是两性氢氧化物 |
| D | 铝具有还原性 | 铝粉和氧化铁粉末可发生铝热反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液中C(A-)=C(R+) |
| B、加入的酸与碱的物质的量相等 |
| C、生成的盐RA不能发生水解 |
| D、加入的一元酸HA过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑤⑥⑨ | B、②⑤⑨ |
| C、①⑤ | D、②⑤⑦⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHC03溶液中存在:c(OH-)=c(H2CO3)+c(H+) |
| B、常温下,pH=3的盐酸和pH=ll的氨水等体积混合后,溶液中:c(NH4+)>c(Cl-) |
| C、0.2mol/L NH4Cl溶液与0.1mol/L NaOH溶液等体积混合后,溶液中:c(NH4+)>c(Na+) |
| D、相同温度下,0.2mol/L的CH3COOH溶液中c(H+)小于0.1mol/L的CH3COOH中c(H+)的两倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com