
(1)9.03×1023个CH4中,含 mol碳原子, mol氢原子,
mol电子。标准状况下,CH4所占的体积为 L。
(2)与17 g NH3所含有分子数相同的氧气的体积(标准状况)是 L。
(3)某3.65 g气体在标准状况下的体积是2.24 L,则其摩尔质量是 。
(4)等质量的氧气和臭氧(O3),它们的物质的量之比为________,所含分子数之比为________,所含原子数之比为________。
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
某化学反应的△H=-122kJ•mol-1,△S=+231J•mol-1•K-1,则此反应在下列哪种情况下可自发进行( )
A.在任何温度下都能自发进行 B.在任何温度下都不能自发进行
C.仅在高温下自发进行 D.仅在低温下自发进行
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理解释的是( )
A.向氯水中加食盐不利于氯气的溶解
B.棕红色NO2加压后颜色先变深后变浅
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.高压有利于合成氨的反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上第一次月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.稀硫酸滴在银片上:2Ag+2H+===2Ag++H2↑
B.稀硫酸与氢氧化钡溶液混合:SO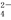 +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C.稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D.氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上第一次月考化学试卷(解析版) 题型:选择题
下列数量的各物质所含原子数按由大到小顺序排列的是( )
①0.5 mol NH3 ②标况下22.4 L He ③18 g水 ④0.8 mol Na3PO4
A.①④③② B.④③②① C.②③④① D.④③①②
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省唐山市高二上10月月考化学试卷 (解析版) 题型:选择题
某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2===2H2O,下列有关说法正确的是( )
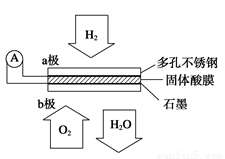
A.电子通过外电路从b极流向a极
B.b极上的电极反应式为O2+2H2O+4e-===4OH-
C.每转移0.1 mol电子,便消耗1.12 L的O2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com