
【题目】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)t℃时,关于N2、NH3的两个反应的信息如下表所示:
化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
N2(g)+O2(g)=2NO(g) △H>0 | a kJ/mol | b kJ/mol | K1 |
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | c kJ/mol | d kJ/mol | K2 |
请写出t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式:______________________,t℃时该反应的平衡常数为__________ (用K1和K2表示)。
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
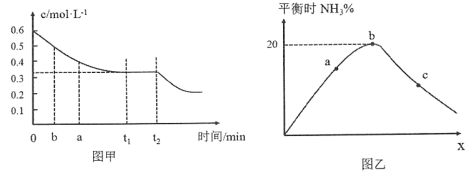
①图甲中0~t1 min内,v(N2)=_____mol·L-1·min-1;b点的v(H2)正_____a点的v(H2)逆(填“大于”“小于”或“等于”)。
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,保持温度和压强不变,又充入3 mol N2后,平衡________(填“向右移动”“向左移动”或“不移动”)。
(3)①科学家研究出以尿素为动力的燃料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,写出负极电极反应式:________________________________________________。
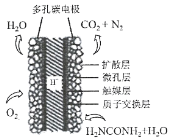
②理论上电池工作时,每消耗标准状况下2.24 L O2时,可产生的电量为________ (法拉第常数为96500C/ mol)。
【答案】4NH3(g)+6NO(g)= N2(g) +6H2O(g) △H=(c-d-5a+5b) kJ/mol K=![]()
![]() mol/(Lmin) 大于 不移动 CO(NH2)2+H2O-6e-=CO2+N2+6H+ 38600c
mol/(Lmin) 大于 不移动 CO(NH2)2+H2O-6e-=CO2+N2+6H+ 38600c
【解析】
(1)已知△H=正反应活化能-逆反应活化能,则①N2(g)+O2(g)=2NO(g) △H=(a-b)kJ/mol >0,②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=(c-d)kJ/mol <0,由盖斯定律知:②-①×5得4NH3(g)+6NO(g)= N2(g) +6H2O(g),据此计算反应△H并写出该反应的平衡常数;
(2) ①图甲中0~t1 min内,H2的变化浓度为0.6mol/L-0.3mol/L=0.3mol/L,由N2(g)+3H2(g)![]() 2NH3(g)可知N2的变化浓度为0.3mol/L×
2NH3(g)可知N2的变化浓度为0.3mol/L×![]() =0.1mol/L,再根据v(N2)=
=0.1mol/L,再根据v(N2)=![]() 计算;根据浓度越大,反应速率越快判断b点与a点的速率大小;
计算;根据浓度越大,反应速率越快判断b点与a点的速率大小;
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,则平衡常数K=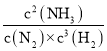 =
=![]() =1,保持温度和压强不变,又充入3 mol N2,此时容器的体积变为2L,则N2、H2和NH3的浓度瞬间变为2mol/L、0.5mol/L和0.5mol/L,根据Qc=
=1,保持温度和压强不变,又充入3 mol N2,此时容器的体积变为2L,则N2、H2和NH3的浓度瞬间变为2mol/L、0.5mol/L和0.5mol/L,根据Qc=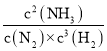 判断平衡移动的方向;
判断平衡移动的方向;
(3)①由尿素燃料电池的结构可知,正极上氧气得到电子生成水,负极上尿素失去电子生成氮气和二氧化碳;
②标准状况下2.24 L O2的物质的量为![]() =0.1mol,转移电子的物质的量为0.4mol,再计算产生的电量。
=0.1mol,转移电子的物质的量为0.4mol,再计算产生的电量。
(1) 已知△H=正反应活化能-逆反应活化能,则①N2(g)+O2(g)=2NO(g) △H=(a-b)kJ/mol >0,②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=(c-d)kJ/mol <0,由盖斯定律知:②-①×5得4NH3(g)+6NO(g)= N2(g) +6H2O(g),即△H=(c-d)kJ/mol -[(a-b)]kJ/mol×5=(c-d-5a+5b) kJ/mol,则t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式为4NH3(g)+6NO(g)= N2(g) +6H2O(g) △H=(c-d-5a+5b) kJ/mol,t℃时此反应的平衡常数为K=![]() ;
;
(2)①图甲中0~t1 min内,H2的变化浓度为0.6mol/L-0.3mol/L=0.3mol/L,由N2(g)+3H2(g)![]() 2NH3(g)可知N2的变化浓度为0.3mol/L×
2NH3(g)可知N2的变化浓度为0.3mol/L×![]() =0.1mol/L,则v(N2)=
=0.1mol/L,则v(N2)=![]() =
=![]() =
=![]() mol/(Lmin);根据浓度越大,反应速率越快可知b点的v(H2)正大于a点的v(H2)逆;
mol/(Lmin);根据浓度越大,反应速率越快可知b点的v(H2)正大于a点的v(H2)逆;
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,则平衡常数K=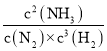 =
=![]() =1,保持温度和压强不变,又充入3 mol N2,此时容器的体积变为2L,则N2、H2和NH3的浓度瞬间变为2mol/L、0.5mol/L和0.5mol/L,根据Qc=
=1,保持温度和压强不变,又充入3 mol N2,此时容器的体积变为2L,则N2、H2和NH3的浓度瞬间变为2mol/L、0.5mol/L和0.5mol/L,根据Qc=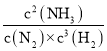 =
=![]() =1=K,则此时平衡不移动;
=1=K,则此时平衡不移动;
(3)①由尿素燃料电池的结构可知,负极上尿素失去电子生成氮气和二氧化碳,负极反应为CO(NH2)2+H2O-6e-=CO2+N2+6H+;
②标准状况下2.24 L O2的物质的量为![]() =0.1mol,转移电子的物质的量为0.4mol,则可产生的电量为96500C/ mol×0.4mol=38600c。
=0.1mol,转移电子的物质的量为0.4mol,则可产生的电量为96500C/ mol×0.4mol=38600c。


科目:高中化学 来源: 题型:
【题目】一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入350mL 2molL﹣1的稀硝酸恰好使混合物完全溶解,放出2.24L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现.若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( )
A. 0.21 molB. 0.25 molC. 0.3 molD. 0.35 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应N2(g)+O2(g)![]() 2NO(g)在密闭容器中进行,达到平衡后,下列措施能改变化学反应速率且能使平衡发生移动的是
2NO(g)在密闭容器中进行,达到平衡后,下列措施能改变化学反应速率且能使平衡发生移动的是
A.恒容,按原平衡各物质的比例充入N2、O2和NOB.恒容,充入He
C.恒压,充入HeD.恒压,充入N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )
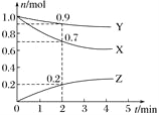
A. X+3Y![]() 2Z 0.1 mol/(L·min) B. 2X+Y
2Z 0.1 mol/(L·min) B. 2X+Y![]() 2Z 0.1 mol/(L·min)
2Z 0.1 mol/(L·min)
C. X+2Y![]() Z 0.05 mol/(L·min) D. 3X+Y
Z 0.05 mol/(L·min) D. 3X+Y![]() 2Z 0.05 mol/(L·min)
2Z 0.05 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲制备摩尔盐[(NH4)2Fe(SO4)2·6H2O]并探究其分解产物。查到如下信息:
摩尔盐可由FeSO4溶液与(NH4)2SO4溶液混合制备;该物质能溶于水、不溶于乙醇,在空气中能逐渐被氧化;100℃开始分解,且分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
I.制备摩尔盐
(1)向新制的FeSO4溶液中加入(NH4)2SO4固体,加热,实验过程中最好采用___________加热方式。
(2)蒸发浓缩、冷却结晶使摩尔盐结晶析出,晶体过滤后用_____________洗涤。
(3)该小组用滴定法测产品纯度。现称取a g该产品于锥形瓶中,加蒸馏水溶解,用0.1000mol/L酸性KMnO4溶液滴定,到达滴定终点时,消耗KMnO4溶液20.00 mL,则该产品的纯度为____________。
II.探究摩尔盐受热分解的产物
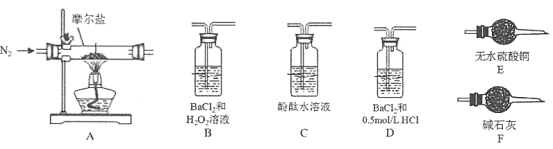
(4)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为___________。(可选部分仪器,填装置的字母序号)
②A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含FeO或Fe3O4______________________。
(5)探究分解产物中的硫氧化物,按A-D-B-F的顺序连接装置,进行实验。
①D装置中试剂的作用是____________________________________________。
②实验过程中,仅B中有沉淀生成,其他实验证明摩尔盐受热分解除上述产物外,还有N2生成。写出摩尔盐受热分解的化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min后达到化学平衡,此时C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1 min-1。
3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min后达到化学平衡,此时C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1 min-1。
(1)5 min末B的物质的量浓度为________。
(2)前5 min内化学反应速率v(A)为_______。
(3)化学方程式中n值为________。
(4)该反应在此温度下的平衡常数K=______(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为__(填“吸热”或“放热”)反应,且m+n_(填“>”“=”或“<”)p。
(2)减压使容器体积增大时,A的质量分数__。(填“增大”“减小”或“不变”,下同)
(3)若升高温度,则平衡时B、C的浓度之比![]() 将___。
将___。
(4)若加入催化剂,平衡时气体混合物的总物质的量____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用水钴矿(主要成分为Co2O3,还含少量Fe2O3、Al2O3、MgO、CaO等杂质)制备钴的氧化物,其制备工艺流程如下(已知Na2SO3能还原Fe3+和Co3+):

回答下列问题:
(1)在加入盐酸进行“酸浸”时,能提高“酸浸”速率的方法有______________(任写2种)。
(2)“酸浸”后加入Na2SO3钴的存在形式为Co2+,产生Co2+反应的离子方程式为________
(3)溶液a中加入NaClO的作用是___________________________________
(4)沉淀a的成分是__________(写化学式),操作2的名称是_______________
(5)溶液d中的金属离子只有Co2+和Na+两种,则溶液c中加入NaF溶液的作用是________
(6)在空气中缎烧CoC2O4生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05g,CO2的体积为6.72L(标准状况),则此反应的化学方程式为____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下,则下列判断正确的是( )
![]()
A.MFe2Ox是氧化剂
B.SO2是该反应的催化剂
C.x<y
D.MFe2Oy是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com