
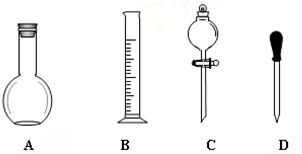
 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.分析 (1)根据配制一定物质的量浓度的溶液实验需要的仪器进行分析;
(2)根据容量瓶的使用方法和注意事项来回答问题;
(3)根据公式m=nM=cvM来计算;根据定容时眼的视线要和凹液面的最低处相平结合公式c=$\frac{n}{V}$来分析误差;
(4)根据稀释前后溶质的质量不变列方程来计算,根据量筒的量取规则来选择.
解答 解:(1)配制一定物质的量浓度的溶液所必需的仪器有:一定规格的容量瓶,托盘天平、烧杯、玻璃棒、胶头滴管,量筒可用可不用,
故答案为:A、C;烧杯、玻璃棒、500mL容量瓶;
(2)根据容量瓶使用时的注意事项:使用容量瓶前检验是否漏水、容量瓶用水洗净后,不能用待配溶液洗涤、不能盛放热溶液、不能作为稀释仪器等,
故答案为:B、C、D;
(3)容量瓶没有450ml,应选择500ml的来配置,据公式m=nM=cvM=0.1mol/L×0.5L×40g/mol=2.0g,若定容时仰视刻度线,则实际溶液体积超过500mL,故所得浓度偏小,
故答案为:2.0g;小于;
(4)设浓硫酸的体积为VmL,稀释前后溶质的质量不变,则:98%×1.84g/cm3V=0.5mol/L×0.50L×98g/mol,解得V=13.6mL,
为减小误差,应选用15mL的量筒,
故答案为:13.6;15.
点评 本题考查了配制一定物质的量浓度的溶液的方法,熟悉配制过程是解题关键,注意误差分析的方法和技巧,题目难度不大.


科目:高中化学 来源: 题型:解答题
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.50 | 20.00 |
| 2 | 0.10 | 18.56 | 20.00 |
| 3 | 0.10 | 18.54 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
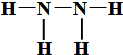
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据分散系是否有丁达尔现象,将分散系分为胶体、浊液和溶液 | |
| B. | 用盐酸可以清洗长期存放过FeCl3溶液的试剂瓶 | |
| C. | 二氧化硅广泛用于制作计算机芯片和光导纤维 | |
| D. | 电解精炼铜时,阳极泥中含有Fe、Ag、Au等金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol冰中有4NA个氢键 | |
| B. | 12克石墨中C---C键为2NA | |
| C. | 氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 | |
| D. | 六方最密堆积中,每个原子的配位数是12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢是铁的一种合金 | |
| B. | 通常合金的硬度比不上纯净的金属 | |
| C. | 合金是两种金属熔合而成的具有金属特性的物质 | |
| D. | 一般地说合金的熔点比它的各成分金属的熔点都高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都是吸热反应 | B. | a、b和c均为正值 | ||
| C. | 反应热的关系:2b=c | D. | 反应热的关系:a=b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
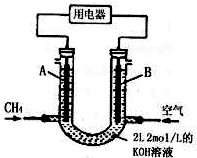 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com