
【题目】氮化铝(AlN)的制取原理为:Al2O3+N2+3C=2AlN+3CO↑,由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质。
(1)称取20.00g样品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,并放出NH36.72L(标准状况)。AlN与NaOH溶液反应的化学方程式为__________;该样品中的的AlN质量分数为__________。
(2)另取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AlN不跟O2反应),该样品中含杂质炭__________g。
【答案】AlN+NaOH+H2O=NaAlO2+NH3↑ 61.5% 1.92
【解析】
(1)AlN跟NaOH溶液反应生成NaAlO2,并放出NH3,以此写出化学方程式,通过氨气的体积计算氨气物质的量,再通过化学方程式计算AlN的质量;
(2)通过![]() ,计算气体平均摩尔质量,判断气体成分,然后根据质量守恒列出等式计算可得。
,计算气体平均摩尔质量,判断气体成分,然后根据质量守恒列出等式计算可得。
(1)AlN跟NaOH溶液反应生成NaAlO2,并放出NH3,则化学方程式为![]() ;NH3物质的量
;NH3物质的量![]() ,则AlN物质的量为0.3mol,AlN质量分数为
,则AlN物质的量为0.3mol,AlN质量分数为![]() ,故答案为:
,故答案为:![]() ;61.5%;
;61.5%;
(2)反应后气体平均摩尔质量![]() ,根据反应
,根据反应![]() ;
;![]() ;
;![]() 可知反应后气体为CO和CO2的混合物,设反应后CO物质的量为xmol,CO2物质的量为ymol,由氧原子质量守恒可得①
可知反应后气体为CO和CO2的混合物,设反应后CO物质的量为xmol,CO2物质的量为ymol,由氧原子质量守恒可得①![]() ,反应后气体平均摩尔质量②
,反应后气体平均摩尔质量②![]() ,由①②解得x=0.14,y=0.02,则反应前C的质量
,由①②解得x=0.14,y=0.02,则反应前C的质量![]() ,故答案为:1.92。
,故答案为:1.92。


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】高锰酸钾是中学常用的试剂。工业上用软锰矿制备高锰酸钾流程。

(1)上述流程中可以循环使用的物质有________、________(写化学式)。
(2)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是________(填代号)。
a.84消毒液(NaClO溶液) b.75%酒精c.苯酚
(3)理论上(若不考虑物质循环与制备过程中的损失)1molMnO2可制得________molKMnO4。
(4)操作Ⅰ的名称是________;操作Ⅱ根据KMnO4和K2CO3两物质在________(填性质)上的差异,采用________(填操作步骤)、趁热过滤得到KMnO4粗晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四溴化乙炔(CHBr2-CHBr2)是一种无色液体,常用于合成季铵化合物.某同学在实验室模仿工业生产,以电石(主要成分CaC2,少量CaS,Ca3P2,Ca3As2等)和Br2等为原料制备少量四溴化乙炔,实验装置(夹持装置已省略)如图所示.已知:四溴化乙炔的熔点为1℃,沸点为244℃,密度为2.967g·cm-3,难溶于水.回答下列问题:
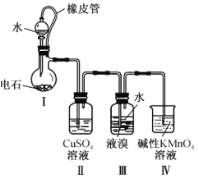
(1)装置Ⅰ中CaC2与水反应生成乙炔(C2H2)和氢氧化钙,写出该反应的化学方程式:__________________;该反应剧烈,为了得到平缓的C2H2气流,可采取的措施是____________(任写一条).
(2)装置Ⅱ的目的是_________________________________________
(3)装置Ⅲ中在液溴液面上加入一层水的目的是__________________________;装置Ⅲ中表明已反应完成的现象是______________________________________________________;已知装置Ⅲ反应后的体系含有多种物质,简述获得纯净四溴化乙炔的操作:________________________________________________
(4)装置Ⅳ的目的是除去未反应的乙炔.在碱性条件下,KMnO4与C2H2反应生成碳酸盐和MnO2,则该反应中参与反应的氧化剂和还原剂的物质的量之比为____________。
(5)实际工业生产中会产生大量的副产物Ca(OH)2,用于制备漂白粉,写出制备漂白粉的化学方程式: _____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物c的制备原理如下:
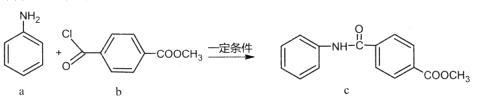
下列说法正确的是
A.该反应为加成反应B.化合物a中所有原子一定共平面
C.化合物C的一氯代物种类为5种D.化合物b、c均能与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80Mpa下合成出了金刚石,具有深远的意义。下列说法错误的是( )
A.该反应是氧化还原反应B.反应中二氧化碳完全被还原为金刚石
C.钠被氧化最终生成碳酸钠D.金刚石是碳的一种同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茉莉醛被广泛应用于食品、化妆品和洗涤剂中。实验室制备茉莉醛的反应:![]() +CH3(CH2)5CHO
+CH3(CH2)5CHO![]()
![]() +H2O,有关数据如下表:
+H2O,有关数据如下表:
相对分子质量 | 密度/g·cm-3 | 沸点/℃ | |
苯甲醛 | 106 | 1.04 | 179 |
庚醛 | 114 | 0.85 | 153 |
茉莉醛 | 202 | 0.97 | 287 |
实验室制备茉莉醛的装置示意图如下:

实验步骤:
在a中加入5.30 mL苯甲醛、5 mL95%乙醇、12 mL10%KOH溶液,在c中加入6.84 g庚醛。搅拌并加热至60~65℃,打开c向a中缓慢滴加庚醛。保温搅拌反应3 h。反应待冷却后,静置分层,分出有机层,水层用20 mL二氯甲烷分两次萃取,萃取分液后与有机层合并,有机层再用10 mL水洗涤3次,洗涤后加入无水Na2SO4。蒸馏,收集287~290℃馏分,馏分用柱色谱法进行分离,得纯净的茉莉醛4.04g。已知:柱色谱分离中,先将液体样品从柱顶加入,流经吸附柱时,即被吸附在柱的上端,然后从柱顶加入洗脱剂,由于吸附剂对各组分吸附能力不同,各组分以不同速度沿柱下移,从而达到分离的效果。
回答下列问题:
(1)仪器a的名称是___________,实验中应采取的加热方法是___________。
(2)在洗涤操作中,用水洗涤的主要目的是________,加入无水Na2SO4的目的是________。
(3)用二氯甲烷萃取分液时,水层在_____(填“上”或“下”)层。
(4)柱色谱法分离中使用的吸附剂为硅胶或碳酸钙,除此之外,还可以使用_______(填序号)
①活性炭 ②氯化钠 ③氧化铝 ④碳酸钾
(5)柱色谱法分离过程中,如果洗脱剂加入速度太快,会使产品产率_______(填“偏高”、“不变”、“偏低”)
(6)本实验所得茉莉醛产率为______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 互为同分异构体,下列说法不正确的是
互为同分异构体,下列说法不正确的是
A. z的二氯代物有三种
B. x、y的一氯代物均只有三种
C. x、y 可使溴的四氯化碳溶液因发生加成反应而褪色
D. x、y、z中只有x的所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备乙酸乙酯的绿色合成路线之一为:

下列说法不正确的是
A. M的分子式为C6H12O6 B. N的结构简式为CH3COOH
C. ④的反应类型属于取代反应 D. 淀粉与纤维素互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com