
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3)3CCH2CH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3CH2)2CHCH3 |
分析 根据等效氢原子来判断各烷烃中氢原子的种类,有几种类型的氢原子就有几种一氯代物,就有几种不同的沸点.
解答 解:根据等效氢的判断方法:同一个碳原子上连的氢原子等效,同一个碳原子上所连的甲基的氢原子等效,对称的碳原子上的氢原子等效.
A.(CH3)2CHCH2CH2CH3含有5种等效氢,所以能生成5种沸点不同的有机物,故A错误;
B.(CH3)3CCH2CH3含有3种等效氢,所以能生成3种沸点不同的有机物,故B正确;
C.(CH3)2CHCH(CH3)2含有2种等效氢,所以能生成2种沸点不同的有机物,故C错误;
D.(CH3CH2)2CHCH3含有4种等效氢,所以能生成4种沸点不同的有机物,故D错误.
故选B.
点评 本题考查同分异构体的判断,注意有几种类型的氢原子就有几种一氯代物,题目难度不大.


科目:高中化学 来源: 题型:解答题
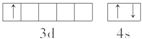 .该元素的原子序数为21,该元素的元素符号是Sc,形成的单质为金属晶体.
.该元素的原子序数为21,该元素的元素符号是Sc,形成的单质为金属晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C3H4 | C. | C2H2 | D. | C3H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐和氯化氢溶于水 | B. | 钠和硫熔化 | ||
| C. | 碘和干冰升华 | D. | 二氧化硅和氧化钠熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
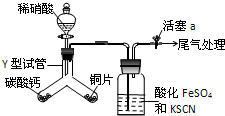 (1)为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.
(1)为探究铜与稀硝酸反应的气态产物中是否含NO2,进行如下实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何溶液中,c(H+)×c(OH-)=1.0×10-14 | |
| B. | pH=0的溶液呈中性 | |
| C. | 酸性溶液中,c(H+)越大,酸性越强 | |
| D. | 酸性溶液中没有OH-,碱性溶液里没有H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com