
Ⅰ.玻璃棒是中学化学实验室中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH ②配制一定物质的量浓度的氯化钠溶液 ③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体 ④探究Ba(OH)2![]() 8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体 ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化 ⑤用蒸馏法分离两种沸点差距较大的液体 ⑥过滤分离互不相溶的固体和液体 ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程 ⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
⑴此方案中,酸碱中和滴定时应选用 滴定管。
⑵写出此方案中涉及到的反应的离子方程式 。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。
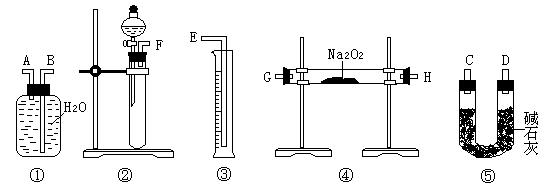
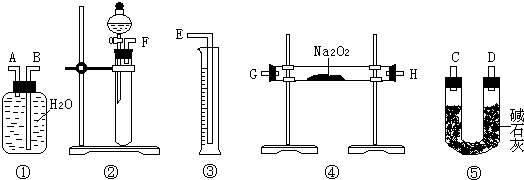
⑶该方案的实验过程中,仪器的连接顺序是 (填仪器下方序号),①中的进气口为 (填“A”或“B”)
⑷装置⑤的作用是 。
⑸你认为方案一、方案二中测定结果比较准确的是 。
Ⅰ③⑤⑦ Ⅱ⑴酸式 ⑵Na2O+H2O=2Na++2OH- 2Na2O2+2H2O=4Na++4OH-+O2↑ H++OH-= H2O ⑶②④⑤①③ A ⑷除去O2中混有的CO2等气体 ⑸方案一
Ⅰ:①的作用是蘸取待测液,②的作用是搅拌和引流,④的作用是搅拌,⑥的作用是引流,⑧的作用是引流;Ⅱ⑴盛盐酸的一定是酸式滴定管;⑵发生的反应是混合物(Na2O和Na2O2)首先与水反应生成氢氧化钠,然后再和盐酸发生中和反应,离子方程式为Na2O+H2O=2Na++2OH- 2Na2O2+2H2O=4Na++4OH-+O2↑ H++OH-= H2O;⑶②制备二氧化碳,④通过过氧化钠固体生成氧气,⑤对氧气进行干燥,①排水法收集氧气,③用量筒量取水的体积就是氧气的体积。(5)方案二:空气中的氧气会对结果带来干扰。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com