
【题目】利用钛白粉厂废酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)制备过二硫酸铵[(NH4)2S2O8],同时回收TiO(OH)2的简要流程如下:

已知:i.部分离子完全生成氢氧化物沉淀的pH
金属离子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
开始沉淀的PH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7时,Fe2+部分生成Fe(II)氨络离子[Fe(NH3)2]2+。
请回答下列问题:
(1)为保证产物TiO(OH)2的纯度,加入试剂A要适量。试剂A为___________。
(2)煅烧回收的TiO(OH)2,获得的TiO2会发黄,发黄的杂质可能是_______(填化学式)。
(3)滤渣I的主要成分除Fe(OH)2、Al(OH)3外,还含有______________。
(4)加入H2O2的目的是氧化除掉Fe(II)氨络离子[Fe(NH3)2]2+,配平下列离子方程式:2[Fe(NH3)2]2+ +________+4H2O +H2O2 =_______ + 4NH3·H2O
(5)电解制备过二硫酸铵的装置如下图所示。

①S2O82-中S元素的化合价为+6,其中过氧键的数目为___________。
②电解时,铁电极连接电源的___________极。
③常温下,电解液中含硫微粒主要存在形式与 pH 的关系如下图所示。

在阳极放电的离子主要为HSO4-,阳极区电解质溶液的 pH 范围为______,阳极的电极反应式为______________________。
【答案】 铁粉 Fe2O3 Fe(OH)3 4OH- 2Fe(OH)3↓ 1 负 0≤pH≤2 2HSO4- - 2e- = S2O82- + 2H+
【解析】(1)铁离子沉淀的PH≤3,而亚铁离子沉淀的PH≤9.4,TiO2+沉淀的PH≤2.8;因此为保证产物TiO(OH)2的纯度,加入适量的铁粉,把铁离子还原为亚铁离子;正确答案:铁粉。
(2)沉淀中会有少量氢氧化铁沉淀掺杂,煅烧后,产生少量的Fe2O3,获得的TiO2会发黄;正确答案:Fe2O3。
(3)滤液中会含有少量的铁离子,加入氨水后,调节溶液的PH=10,会产生Fe(OH)2、Al(OH)3外,还含有少量的Fe(OH)3;正确答案:Fe(OH)3。
(4)[Fe(NH3)2]2+中铁为+2价,被氧化为+3价铁,在碱性环境下生成Fe(OH)3,H2O2中氧由-1价降低到-2价,发生还原反应,根据化合价升降总数相等,电荷守恒规律,配平后的离子方程式:2[Fe(NH3)2]2+ +4OH-+4H2O +H2O2 = 2Fe(OH)3↓+ 4NH3·H2O;正确答案:4OH- ;2Fe(OH)3↓。
(5)①S2O82-中硫元素为+6,氧为-2价,过氧根中氧元素为-1价,设过氧键的数目为x,根据化合价法则可知:6×2+(-2)×(8-2x)+(-1) ×2x=-2,解得x=1,正确答案:1。
②电解池中,HSO4-在阳极失电子发生氧化反应,生成S2O82-,如果铁做阳极,铁失电子,HSO4-就不能失电子,也就不能生成二硫酸铵[(NH4)2S2O8],因此铁做电解池的阴极,与电源的负极相连;正确答案:负。
③根据图示可知,在阳极放电的离子主要为HSO4-,阳极区电解质溶液的 pH 范围为0≤pH≤2;HSO4-失电子变为S2O82-,发生氧化反应,阳极的电极反应式为2HSO4- - 2e- = S2O82- + 2H+;正确答案:0≤pH≤2;2HSO4- - 2e- = S2O82- + 2H+。


科目:高中化学 来源: 题型:
【题目】碱性锌锰电池的工作原理:Zn+2MnO2+2H2O![]() 2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1x)Fe2O4,其工艺流程如图所示:
2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1x)Fe2O4,其工艺流程如图所示:

(1)已知MnxZn(1x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为___________。
(2)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:_________________________________。
(3)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:______________________、_______。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L1,c(Fe2+)+c(Fe3+)=b mol·L1,滤液体积为1 m3,“调铁”工序中,需加入的铁粉质量为___________kg(忽略溶液体积变化,用含a、b的代数式表示)。
(4)在“氧化”工序中,加入双氧水的目的是把 Fe 2+ 氧化为 Fe 3+;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是______________________。
(5)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是研究二氧化硫性质的微型实验装置.现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )

A. 紫色石蕊溶液先变红后褪色B. 品红溶液褪色
C. 溴水橙色褪去D. 含酚酞的NaOH溶液红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知反应2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436KJ、151KJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(2)某温度下,浓度都是l mol/L的两种单质气体X2和Y2,在密闭容器中反应生成气体Z。达到平衡时,X2、Y2、Z的浓度分别为0.4mol/L、0.8mol/L、0.4mol/L则该反应的化学方程式是____________________________。
(3)对反应N2O4(g)![]() 2NO2(g) △H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是______。
2NO2(g) △H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是______。

a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A<C
d.由状态B到状态A,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0达平衡后,改变某一反应条件,反应速率随时间变化的情况。根据曲线判断下列说法中正确的是
2NH3(g) ΔH<0达平衡后,改变某一反应条件,反应速率随时间变化的情况。根据曲线判断下列说法中正确的是
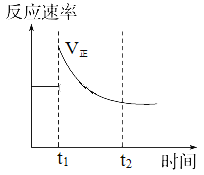
A. t1时降低了温度,平衡向正反应方向移动
B. t1时增大了压强,平衡向正反应方向移动
C. t1时增大了N2的浓度同时减小了NH3的浓度,平衡向正反应方向移动
D. t1时可能使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把镁条投入到盛有盐酸的敞口容器里,产生H2的速率如图所示。在下列因素中,能影响此反应速率的因素是( )

①盐酸的浓度 ②镁条的表面积
③溶液的温度 ④Cl-的浓度
A.①④B.②③C.①②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的描述中,正确的是
①钠放入水中后,沉在水下缓缓冒出气体
②Na2CO3和NaHCO3的溶液都可以使无色酚酞试液变红
③氢气在氧气或氯气中燃烧,都能观察到淡蓝色火焰
④将某气体通入品红溶液中,红色褪去,说明该气体一定是SO2
⑤向某溶液中加入烧碱溶液,加热后生成使湿润红石蕊试纸变蓝的气体,说明原溶液中有NH4+。
⑥过氧化钠与水反应放出大量热
A. ①③⑥ B. ②④⑤ C. ②⑤⑥ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是
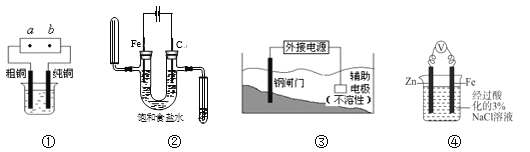
A. 用装置①精炼铜,则a极为电源正极,电解质溶液可为CuSO4溶液
B. 用湿润的淀粉-KI试纸检验装置②中阳极气体产物时,试纸变为蓝色
C. 装置③中钢闸门应与外接电源的负极相连,该保护法称为“牺牲阳极的阴极保护法”
D. 装置④中反应一段时间后,取Fe电极附近溶液滴加铁氰化钾溶液,不会产生蓝色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质

(1)Ti是一种活泼金属,原子核内有22个质子,它在周期表中的位置是____________。
(2)根据上表信息推测TiCl4中含有的化学键类型是_______________。
(3)MgCl2的电子式为____________。
(4)氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有_________________。
(5)精制过程:粗TiCl4经两步蒸馏得纯TiCl4如图。

①物质a是__________________(填化学式)。
②T1应控制在______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com