
【题目】已知a An+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
A. 原子序数:b>a>c>dB. 最高价氧化物对应水化物的碱性:B>A
C. 四种离子的电子层结构相同,因而离子的性质也相同D. 气态氢化物的稳定性:D>C
【答案】A
【解析】
a An+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则在周期表中的相对位置是 ,据此分析作答。
,据此分析作答。
A. 根据A、B、C、D在周期表中的相对位置,可知原子序数:b>a>c>d,故A正确;
B.元素金属性越强最高价氧化物的水化物的碱性越强,同周期元素从左到右元素金属性减弱,金属性A>B,最高价氧化物对应水化物的碱性:A>B,故B错误;
C. a An+、bB(n+1)+具有氧化性,cCn-、dD(n+1)-具有还原性,所以四种离子的性质不同,故C错误;
D. 同周期从左到右非金属元素气态氢化物的稳定性增强,所以气态氢化物的稳定性C>D,故D错误。答案选A。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。则下列说法中正确的是 ( )
⑴ 0.25 mol Na2O2中含有的阴离子数为0.5NA
⑵ 7.5 g SiO2晶体中含有的硅氧键数为0.5 NA
⑶ 标准状况下,2.24 L CCl4中含有的原子数为0.1 NA
⑷ 常温下,1 L 0.1 mol/L FeCl3溶液中含Fe3+数为0.1NA
⑸ 1 L 1 mol/LCH3COOH溶液中含有NA个氢离子
⑹ 常温下,2.7 g铝与足量的氢氧化钠溶液反应,失去的电子数为0.3NA
⑺ 22.4 L SO2气体,所含氧原子数为2NA
⑻ 14 g乙烯和丙烯的混合物中,含有共用电子对数目为3 NA
⑼ 25℃时,pH =13 的1.0 LBa(OH) 2 溶液中含有的OHˉ数为0.2NA
A. ⑵⑸⑻⑼ B. ⑵⑹⑻ C. ⑴⑷⑹⑻⑼ D. ⑴⑶⑸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述不正确的是
A. 通常状况下,1 mol SO3含有的分子数为NA
B. 1 mol OH-参与电解,转移的电子数目为NA
C. 标准状况下,含NA个氩原子的氩气体积约为22.4 L
D. 标准状况下,V L水含有的氧原子数约为VNA/22.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质焰色均为黄色,它们按图所示互相转化.

(1)这五种物质中,A:______、C:______.
(2)将CO2通入E的饱和溶液中,该反应的离子方程式为__________________________.
(3)写出A→D、C→D反应的化学方程式
A→D:______________________________
C→D:______________________________
(4)现将C与NaHCO3固体按物质的量之比为3:2于真空密闭容器中混合加热,则剩余固体成分为_______________。
(5)将a g葡萄糖在足量氧气中完全燃烧,将所得产物全部通入过量C中,固体增重________a g。(填大于,小于,等于)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验法是学习化学的重要方法。
Ⅰ.海带中含有丰富的碘元素,以碘离子的形式存在。实验室里从海藻中提取碘的流程如下(已知2I-+Cl2=2Cl-+I2,碘与溴一样易溶于有机溶剂):

(1)实验操作①的名称:___________________ 。
(2)实验步骤②中加适量Cl2的目的是______________________________。
(3)实验步骤③提取碘的过程中,不能选用的溶剂是________。
A.苯 B.酒精 C.四氯化碳
(4)从海藻开始经过5步操作到含碘的有机溶液的实验过程中,要用到多种实验仪器。已知实验室里有坩埚、坩埚钳、烧杯、玻璃棒、酒精灯、石棉网、以及必要的夹持仪器等物品,尚缺少的玻璃仪器是__________________、________________。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出下图所示实验装置中的错误之处:_________________、_________________、__________________。

Ⅱ.某学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物:

填空和回答下列问题
(1)写出生成B物质的化学方程式________________
(2)滤液中的溶质有_____________________(写化学式),若要制得纯净的NaCl,应向滤液中加入适量的某种试剂,该试剂的名称是_________________ 。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰) Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1-36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
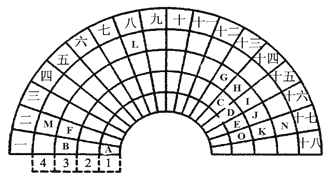
(1) D代表的元素处于常见元素周期表的位置是第 _____ 周期________ 族。
(2)元素F、G、I、K、M的原子半径由大到小的顺序是___________________(用元素符号表示)。
(3)B、F、G三种元素三种元素最高价氧化物对应水化物碱性最强的碱是_________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各溶液中的反应,不论反应物量的多少,都只能用同一个离子方程式来表示的是
A.FeBr2与Cl2B.Ba(OH)2与CO2
C.HCl与Na2CO3D.AlCl3与氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池在我们的生活中有着重要的应用,请回答下列问题:
(1)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是______(填序号),写出正极的电极反应式_______。若构建原电池时两个电极的质量相等,当导线中通过0.05mol电子时,两个电极的质量差为________。

(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。

实验测得OH定问移向B电极,则_____(填“A”或“B”)处电极入口通甲烷,其电极反应式为___________。当消耗甲院的体积为33.6 L(标准状况下)时,假设电池的能量转化率为80%,则导线中转移电子的物质的量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com