
| A、CH2=CH-CH2-CH3 |
| B、CH2=C(CH3) CH=CH2 |
| C、(CH3)2CHCH=CH2 |
| D、(CH3)3CCH═CH2 |
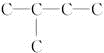 ,A可能含一个三键或两个双键或一个双键,若为炔烃,则为
,A可能含一个三键或两个双键或一个双键,若为炔烃,则为 ,3-甲基-1-丁炔;若为二烯烃,存在两个C═C,则结构简式为
,3-甲基-1-丁炔;若为二烯烃,存在两个C═C,则结构简式为 ,2-甲基-1,3-丁二烯,故B正确;
,2-甲基-1,3-丁二烯,故B正确;

科目:高中化学 来源: 题型:
| 1 |
| 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
| D、乙酸(乙醇):加入金属钠,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 是世界通用的循环再生标志,简称回收标志 是世界通用的循环再生标志,简称回收标志 |
| B、含有食品添加剂的食品对人体健康均有害,不宜食用 |
| C、硫、氮的氧化物会造成酸雨,酸雨指pH小于7的雨水 |
| D、明矾是常用的水处理剂,可用于城市自来水的杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)下列说法正确的是( )
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-)下列说法正确的是( )| A、该温度下,Ksp(BaSO4)=1.0×10-24 |
| B、a点的Ksp(BaSO4)小于b点的Ksp(BaSO4) |
| C、d点表示的是该温度下BaSO4的不饱和溶液 |
| D、加入BaCl2可以使溶液由c点变到a点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、水解反应NH4++H2O?NH3?H2O+H+达到平衡后,升高温度平衡逆向移动 |
| C、制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D、盐类水解反应的逆反应是中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
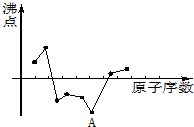
| A、C | B、Na | C、Ne | D、N |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com