

分析 由流程图可知,废旧线路板有铜,试剂a要满足可以把铜单质氧化生成硫酸铜、不引入关键杂质离子(例如Fe2+、Fe3+)且不污染环境等条件,由已知终端产物金属铜和硫酸铁溶液反推可知固体X为铁和铜,溶液Y为FeSO4溶液,从而确定试剂b为Fe,废旧电路板也可以加入试剂c溶解,试剂c为硫酸铁,用来溶解铜生成硫酸亚铁和硫酸铜,得到混合溶液Z,在溶液中加入铜除去过量硫酸铁,分离得到硫酸铜溶液和硫酸亚铁溶液Y,固体X为铁和铜,加入稀硫酸溶解铁,过滤得到金属铜和滤液Y,在滤液Y中加入氧化剂氧化硫酸亚铁为硫酸铁,在碱性溶液这通入氯气氧化硫酸铁为高铁酸钾;
(1)试剂a要满足可以把铜单质氧化生成硫酸铜、不引入关键杂质离子(例如Fe2+、Fe3+)且不污染环境等条件,废旧电路板与试剂a反应能够生成硫酸铜溶液的有A、B、D三种试剂,但A浓硫酸与铜反应就需要加热,而且反应还会产生SO2污染空气,B硫酸铁溶液与铜反应会产生Fe2+、Fe3+杂质离子;D选项利用过氧化氢做氧化剂在酸溶液中氧化铜生成硫酸铜,无污染;
(2)由CuSO4溶液和溶液Y(FeSO4溶液)可知试剂c为硫酸铁溶液,KMnO4溶液可腐蚀橡胶;
(3)Cu+HCl+O2=CuCl+HO2中,Cu元素的化合价由0升高为+1价,由HO2不仅是一种弱酸而且也是一种自由基,具有极高的活性可知O元素的化合价降低;
(4)洗涤剂的选择要求:要对K2FeO4水解能起到抑制作用的试剂,K2FeO4除与水反应生成4Fe(OH)3(胶体)之外,还具有强氧化性,FeCl3净水是由于Fe3+生成Fe(OH)3胶体;
(5)在碱性溶液这通入氯气氧化硫酸铁为高铁酸钾.
解答 解:由流程图可知,废旧线路板有铜,试剂a要满足可以把铜单质氧化生成硫酸铜、不引入关键杂质离子(例如Fe2+、Fe3+)且不污染环境等条件,由已知终端产物金属铜和硫酸铁溶液反推可知固体X为铁和铜,溶液Y为FeSO4溶液,从而确定试剂b为Fe,废旧电路板也可以加入试剂c溶解,试剂c为硫酸铁,用来溶解铜生成硫酸亚铁和硫酸铜,得到混合溶液Z,在溶液中加入铜除去过量硫酸铁,分离得到硫酸铜溶液和硫酸亚铁溶液Y,由已知硫酸铁溶液反推可知溶液Y为FeSO4溶液,由CuSO4溶液与试剂b反应生成FeSO4溶液和固体X不难推出试剂b为Fe,固体X为铜和过量铁粉,加入稀硫酸溶解铁,过滤得到金属铜和滤液Y,在滤液Y中加入氧化剂氧化硫酸亚铁为硫酸铁,在碱性溶液这通入氯气氧化硫酸铁为高铁酸钾;
(1)试剂a要满足可以把铜单质氧化生成硫酸铜、不引入关键杂质离子(例如Fe2+、Fe3+)且不污染环境等条件,废旧电路板与试剂a反应能够生成硫酸铜溶液的有A、B、D三种试剂,但A浓硫酸与铜反应就需要加热,而且反应还会产生SO2污染空气,B硫酸铁溶液与铜反应会产生Fe2+、Fe3+杂质离子;D选项利用过氧化氢做氧化剂在酸溶液中氧化铜生成硫酸铜,反应的离子方程式为:Cu+H2O2+2H+=Cu2++2H2O,
故答案为:D;Cu+H2O2+2H+=Cu2++2H2O;
(2)由CuSO4溶液和溶液Y(FeSO4溶液)可知试剂c为硫酸铁溶液,2Fe3++Cu=2Fe2++Cu2+;Fe3+与SCN-反应生成红色的Fe(SCN)3,通常用KSCN溶液来检验Fe3+;一定物质的量浓度溶液的配制实验用到的主要仪器就是容量瓶,KMnO4溶液具有强氧化性,可腐蚀橡胶管,所以强氧化性及酸性溶液应加入酸式滴定管,
故答案为:容量瓶;酸式;
(3)A.O元素的化合价降低,则氧化剂是O2,故A正确;
B.HO2是一种弱酸,与碱反应,则在碱中不能稳定存在,故B正确;
C.O得到电子被还原,则还原产物是HO2,故C错误;
D.1mol Cu参加反应有1mol×(1-0)=1mol电子发生转移,故D正确;
故答案为:C;
(4)洗涤剂的选择要求:要对K2FeO4水解能起到抑制作用的试剂,在选项中,A能让K2FeO4水解,B中醋酸钠水解显碱性,对K2FeO4水解能起到抑制作用,C和D中的铵根和三价铁离子易水解,且水解后显酸性,对K2FeO4水解能起到促进作用,故选B,FeCl3净水是由于Fe3+生成Fe(OH)3胶体,Fe(OH)3胶体能吸附水中的悬浮物而达到净水目的,K2FeO4除与水反应生成Fe(OH)3(胶体)之外,还具有强氧化性,可以杀菌消毒,处理水的效果更好的是K2FeO4,
故答案为:B;K2FeO4;高铁酸钾(K2FeO4)具有强氧化性,在净水的同时还能杀菌消毒;
(5)在碱性溶液这通入氯气氧化硫酸铁为高铁酸钾,生成K2FeO4的离子方程式2Fe3++3Cl2+16OH-=2 FeO42-+6Cl-+8H2O,
故答案为:2Fe3++3Cl2+16OH-=2 FeO42-+6Cl-+8H2O.
点评 本题考查铜、铁及其重要化合物、Fe3+检验、容量瓶滴定管的使用、净水原理、转移电子的计算、电极反应式的书写等知识,考查综合全面,熟知铜、铁单质及其离子的转化是解题关键,转移电子的计算和正极电极反应式的书写是难点,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2 mol SO2与1 mol O2能完全反应生成2 mol SO3,升高温度可以加快此反应的化学反应速率 | |
| B. | 2 mol SO2与1 mol O2不能完全反应生成2 mol SO3,升高温度可以加快此反应的化学反应速率 | |
| C. | 2 mol SO2与1 mol O2能完全反应生成2 mol SO3,升高温度减慢此反应的化学反应速率 | |
| D. | 2 mol SO2与1 mol O2不能完全反应生成2 mol SO3,升高温度减慢此反应的化学反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同族元素,随着电子层的增加,I1逐渐增大 | |
| B. | 通常情况下,电离能I1<I2<I3 | |
| C. | 同周期元素,随着核电荷数的增加,I1呈增大趋势 | |
| D. | 电离能越小,元素的金属性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都有酸性,电离出的H+有弱氧化性 | |
| B. | 它们都是酸,彼此之间不发生反应 | |
| C. | 亚硫酸易分解放出SO2,所以它是挥发性酸 | |
| D. | 在空气中放置,它们都会因氧化而变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )
白磷与氧气可发生如下反应:P4+5O2═P4O10.已知断裂下列1mol化学键需要吸收的能量分别为:P-P a kJ、P-O b kJ、P=O c kJ、O=O d kJ.根据下图所示的分子结构和有关数据估算1mol P4发生该反应放出的热量是( )| A. | (6a+5d-4c-12b) kJ | B. | (4c+12b-6a-5d) kJ | C. | (4c+12b-4a-5d) kJ | D. | (5a+5d-4c-12b) kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
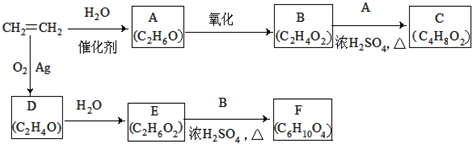
 .
.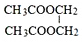 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每生成2mol SO2的同时,消耗2molSO3 | |
| B. | 混合气体的总质量不再变化 | |
| C. | 每生成2mol SO3的同时,消耗1molSO2 | |
| D. | 混合气体的压强不再变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com