
【题目】某有机化合物A的结构简式如下:
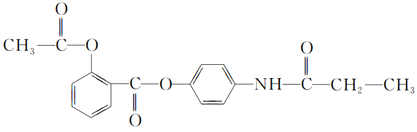
(1)A的分子式是________。
(2)A在NaOH水溶液中充分加热后,再加入过量的盐酸酸化后,可得到B、C、D和![]() 四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
四种有机物,且相对分子质量大小关系为B>C>D,则B、C、D的结构简式分别是B________;C________;D________。
(3)下列物质中,不能与B发生化学反应的是________(填空序号)。
①浓H2SO4和浓HNO3的混合液 ②CH3CH2OH(酸催化) ③CH3CH2CH2CH3 ④Na ⑤浓溴水
(4)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式为_________________。
(5)写出B与碳酸氢钠反应的化学方程式:___________________。
【答案】 C18H17O5N ![]() CH3CH2COOH CH3COOH ③
CH3CH2COOH CH3COOH ③ 
【解析】本题主要考查羧酸类物质的性质。
(1)A的分子式是C18H17O5N。
(2) B、C、D分别是邻羟基苯甲酸、丙酸、乙酸,B、C、D的结构简式分别是A.![]() ;B.CH3CH2COOH;C.CH3COOH。
;B.CH3CH2COOH;C.CH3COOH。
(3)B是邻羟基苯甲酸。①浓H2SO4和浓HNO3的混合液与B发生硝化反应;②CH3CH2OH(酸催化)与B发生酯化反应;③CH3CH2CH2CH3不能与B发生反应;④Na与B发生置换反应;⑤浓溴水与B发生取代反应。故选③。
(4)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式为 。
。
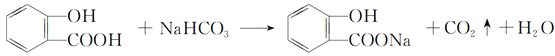
(5)酸性:B中—COOH>H2CO3>酚羟基,所以B与碳酸氢钠反应是B的羧基与碳酸氢钠的反应,反应的化学方程式:![]() 。
。


科目:高中化学 来源: 题型:
【题目】
K、Fe、Ni均为重要的合金材料,在工业生产、科技、国防领域有着广泛的用途,请回答下列问题:
(1)K元素处于元素周期表的_____ 区,其基态原子中,核外电子占据的电子云轮廓图为球形的能级有______个。
(2)KCl 和NaCl 均为重要的化学试剂,KCl 的熔点低于NaCl的原因为___________。
(3)从原子结构角度分析,Fe3+比Fe2+更稳定的原因是__________。
(4)NiSO4 溶于氨水形成[Ni (NH3)6]SO4。
①写出一种与[Ni(NH3)6]SO4中的阴离子互为等电子体的分子的分子式_________。
②1mol[Ni(NH3)6]SO4中含有σ键的数目为___________。
③NH3 的VSEPR模型为_____ ;中心原子的杂化形式为_____,其杂化轨道的作用为__________。
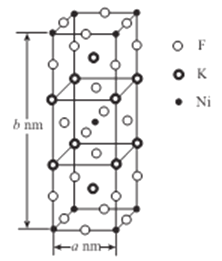
(5)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加德罗常数的值,该晶体的密度ρ=______g/cm3(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物比卡鲁安(G)可以通过以下方法合成:
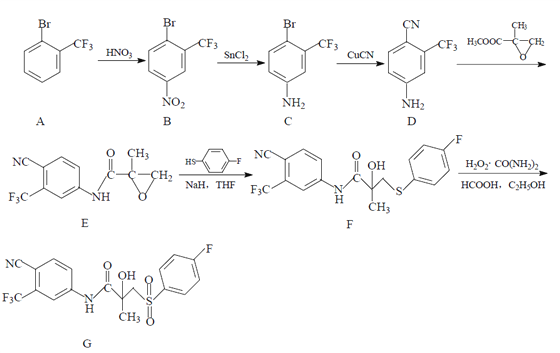
(1)B 中的含氧官能团名称为 _______________ ;
(2)C→D的反应类型为 __________________ ;
(3)写出同时满足下列条件的 D 的一种同分异构体的结构简式:_______________ ;
①有苯环;②能使溴的 CCl4 溶液褪色;③分子中有 2 种不同化学环境的氢
(4)合成 F 时还可能生成一种副产物 X,X 的结构简式为 _________________ ;
(5)已知 : 苯胺 (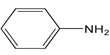 ) 易被氧化,请以甲苯和甲醇为原料制备
) 易被氧化,请以甲苯和甲醇为原料制备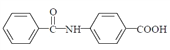 。________________
。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(I)写出下列反应的热化学方程式。
(1)N2(气态)与H2(气态)起反应,完全反应生成34g NH3(气态)放出92.2 kJ的热量:________________________________________。
(2)标况下22.4L N2(气态)与适量O2(气态)起反应,生成NO(气态)需吸收68 kJ的热量:______________________________________。
(3)卫星发射时可用肼(N2H4)为燃料,1 mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534 kJ的热量:__________________________________________。
(4)已知断裂1 mol H—H键、1 mol N≡N键分别需要吸收436 kJ、946 kJ的能量,生成1 mol N—H键放出391 kJ的能量,试写出N2(g)与H2(g)反应生成NH3(g)的热化学方程式:___________________________________。
(II)已知: C(s)+ O2(g) === CO2(g) ΔH=-393.5 kJ/mol
2CO(g)+O2(g) === 2CO2(g) ΔH=-566 kJ/mol
TiO2(s)+2Cl2(g) === TiCl4(s)+O2(g) ΔH=+141 kJ/mol
则TiO2(s)+2Cl2(g)+2C(s) === TiCl4(s)+2CO(g) ΔH= __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一酸两浸,两碱联合”法是实现粉煤灰(含SiO2、Al2O3、Fe2O3、CaO、MgO等)综合利用的新工艺。工业流程如下:

回答下列问题:
(1)聚合氯化铝铁(PAFC)化学式为[Al2(OH)nCl6-n]m·[Fe2(OH)xCl6-x]y,是一种新型高效的净水剂,PAFC中铁元素的化合价为___________。
(2)“一酸两浸”中的酸是________________(填结构式)。
(3)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为_____________、 ________________。
(4)“滤液B”的主要溶质有_____________(填化学式)。滤液混合后“蒸发”的作用是____________________________________。
(5)“电解”时的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】磷是人体含量较多的元素之一,磷的化合物在药物生产和农药制造等方面用途非常广泛。回答下列问题:
(1)基态磷原子核外共有________个未成对的电子。
(2)P4S3可用于制造火柴,其结构如图所示。

①电负性:磷_______硫;第一电离能:磷_______硫; (填“>”或“<)。
②P4S3中硫原子的杂化轨道类型为_______。
(3)N、P、As、Sb均是第VA族的元素。
①上述元素的氢化物的沸点关系如图乙所示,沸点:PH33,原因是_______;沸点:PH333,原因是_______。
②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为_______。
(4)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图丁所示。
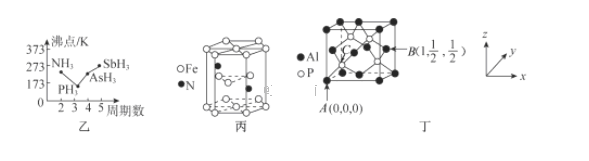
①图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为_______。
②磷化铝晶体的密度为ρg·cm-3用NA表示阿伏加德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为_______cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全。确定分解产物的成分。

(1)B装置的作用是________________________________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中定有______气体产生,写出D中发生反应的离子方程式____________________。若去掉C,是否能得出同样结论并解释其原因__________________________。
(3)A中固体分解后产生NH3,写出其两种用途________________________________________。
(4)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3而不含FeO。请完成表内容。(试剂,仪器自选)
实验步骤 | 预期现象 | 结论 |
①取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解; ②______________________________________________________ | 固体残留物仅为Fe2O3 |
(5) 用实验的方法验证C溶液含有NH4+___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.3 mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2 mol。试回答:
(1)烃A的分子式为_____________。
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则有________g烃A参加了反应,燃烧时消耗标准状况下的氧气___________L。
(3)若烃A跟HCl反应后,生成产物中的H原子的结构环境完全相同,写出该反应的化学方程式_____。
(4)若烃A与Br2的CCl4溶液反应后的产物为1,2-二溴丁烷,请写出由烃A发生加聚反应的化学方程式_________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com