
在一密闭容器中,进行mX(g)+nY(s) ![]() 3Z(g);△H<0的反应,下列说法正确的是( )
3Z(g);△H<0的反应,下列说法正确的是( )
A.加入催化剂可以提高X的转化率
B.缩小容器的体积,混合体系中X的含量增加,则m一定小于3
C.降低温度,正反应速率增大,逆反应速率减小,混合体系中Z的含量增大
D.加入一些Y,平衡向右移动,可以提高X的转化率
科目:高中化学 来源: 题型:阅读理解
| T | 298K | 398K | 498K | … |
| K | 4.1×106 | K1 | K2 | … |
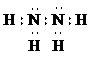
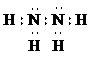
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| T/K | 298 | 398 | 498 |
| K | 4.1×106 | K1 | K2 |

| O |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中,进行mX(s)+nY(g)![]() 2Z(g);ΔH=Q的反应中,下列结论正确的是( )
2Z(g);ΔH=Q的反应中,下列结论正确的是( )
A.缩小容器的体积,发现混合气体的密度增大,则n一定大于2
B.加入一些X,平衡一定往右移动,可以提高Y的转化率
C.升高温度,正反应、逆反应速率同时增大,X和Y的质量增加,说明Q>0
D.若增大压强,Z的百分含量不变,则m+n>2
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素有着多变价态和种类繁多的化合物,它们在工农业生产、生活中发挥着重要的作用。完成下列问题:
(1)在一密闭容器中,进行如下化学反应:
N2(g)+3H2(g)![]() 2NH3(g) △H<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与温度T的关系如下表:
| T | 298 K | 398 K | 498 K | … |
| K | 4.1×106 | K1 | K2 | … |
①比较K1、K2的大小:K1______K2(填“>”、“=”或“<”)。
②若保持容器的容积不变,则该反应达到化学平衡状态的依据是________(填序号)。
a.2v(H2)正=3v(NH3)逆 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的平均摩尔质量保持不变
③若维持容器的压强不变,达到平衡状态后再向容器中通入一定量的N2,此时逆反应速率______(填“增大”、“减小”或“不变”);平衡向_____方向移动。
④已知AgCl可溶于氨水中,而AgBr不溶于氨水中,则Ksp(AgCl)______ Ksp(AgBr)。
( 2 )肼是氮元素的另一种氢化物,分子式为N2H4。
①298 K时,1.00 g N2H4(l)与足量的N2O4(l)完全反应生成氮气和水,放出19.15 kJ的热量。写该反应的热化学方程式_____________________________________。
②肼也可以在纯氧中燃烧生成氮气和水,为了充分利用其能量有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com